멸종위기 붉은박쥐(Myotis rufoniger)의 행동권 크기 및 서식지 이용 특성
Ⓒ The Korean Environmental Sciences Society. All rights reserved.
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
The present study investigated the home range and habitat use of Myotis rufoniger within and around a designated conservation area from May to October 2025. The mean home range size was 5.68 ± 5.35 km² (0.64–18.38 km²), and the mean movement distance from the conservation area was 4.94 km (1.82–11.96 km). Among the 16 tracked individuals, only 18.8% (three bats) used > 50% of their home range within the conservation area, whereas the remaining 81.2% (13 bats) used 0–38% of the conservation area. Seasonal home range size was the largest in summer (11.71 ± 6.04 km²), followed by autumn (6.15 ± 2.16 km²) and spring (2.42 ± 3.27 km²). Females exhibited significant seasonal variation in home range size, whereas males did not. Core area size averaged 0.81 ± 0.73 km², accounting for approximately 18.4% of the total home range. The mean elevation within home ranges was < 160 m, and > 60% of habitat use occurred at < 200 m. No distinct aspect trend was observed, although many individuals used flat terrain preferentially. In addition, bats favored low-slope areas, and they used forests, aquatic habitats, and agricultural land frequently. The findings of the present study provide key quantitative insights into M. rufoniger spatial ecology, highlighting the need for conservation planning that extends beyond hibernacula to include landscape connectivity and protection of external core habitats.
Keywords:
Conservation planning, Core habitat, Habitat use, Home range, Myotis rufoniger, Spatial ecology1. 서 론
박쥐는 곤충의 주요 포식자로서 우리나라와 같이 온대지역에 서식하는 식충성 박쥐는 생태계에서 해충 밀도 조절에 핵심적 역할을 수행하며, 생태계 안정성과 농업 생산성 유지에 기여한다(Chung, 2020). 또한 과일이나 꿀을 먹이원으로 하는 박쥐는 꽃가루 매개와 종자 분산의 주요 매개체로서 열대·온대림의 식물군집 구조와 재생을 결정짓는 역할을 한다(Kunz et al., 2011). 박쥐는 많은 종이 동굴이나 폐광, 고목, 기타 인공구조물을 이용함으로써 서식지 건강성을 평가할 수 있는 지표종 기능을 하며, 박쥐 개체군의 변화는 지역 생태계의 교란 여부를 반영하는 중요한 생태학적 시그널로 활용된다(Humphries et al., 2002).
본 연구대상인 붉은박쥐(Myotis rufoniger)는 우리나라를 포함하여 베트남, 라오스, 대만, 중국, 일본 등 동아시아에 분포하며, 선명한 오렌지색깔을 띠는 특징이 있다. 우리나라에서는 개체군 규모가 제한적이고 전국 분포 또한 국지적으로 이루어지고 있어 멸종위기종으로 분류되고 있다(Chung, 2020). 동면기에는 동굴이나 폐광을 이용하며, 여름철 활동기에는 울창한 산림지역을 활동공간으로 이용하는 종으로, 기타 박쥐류와 비교하여 동면기간이 길고 동면처 온습도의 선호범위가 좁은 특징이 있다(Chung, 2020).
지금까지 붉은박쥐에 관한 선행연구는 주로 동면기를 중심으로 수행되었으며, 동면처의 미기후 특성과 기타 동면생태에 관한 정보가 대부분을 차지하고 있다(Kim et al., 2009). 이러한 이유로 20여년 전부터 붉은박쥐 개체군 보호를 위해 무선추적을 이용한 활동기 행동권 범위파악 및 밴딩을 통한 생태연구의 필요성이 제기되어 왔음에도 불구하고 이와 관련된 연구는 거의 이루어지지 않았다(YBEO, 2006). 동면처 환경 및 동면생태에 관한 연구는 붉은박쥐의 동면 생리와 동면처 조건을 이해하는데 유용하지만, 종의 연중 활동과 공간 이용특성을 파악하기에는 한계가 있으며, 이처럼 특정 분야로 편중된 연구는 실제 보전활동 또한 동면처 관리에 집중되도록 유도하여, 종의 연중 생태를 반영한 포괄적 보전 전략 수립에 편향을 초래할 수 있다.
행동권 정보는 채식지의 위치, 서식지 연결성, 핵심 공간의 환경요인을 규명하는데 필수적인 기반 자료로서, 종의 서식지 이용 전략을 해석하는데 중요한 역할을 한다(Boyles et al., 2007). 뿐만 아니라 활동기 서식지 환경특성 분석은 산림내 서식지 구조, 먹이자원 분포, 경관 연결성 등 종의 서식지 선택을 결정하는 핵심 요인을 규명하여 효과적인 보전지역 설정과 서식지 복원 방향을 제시하는 데 중요한 근거를 제공한다(Fenton and Simmons, 2014). 이러한 공간생태 자료가 부족할 경우, 서식지 파편화와 환경 변화에 대한 취약성을 제대로 평가하기 어려우며, 보전 조치의 우선순위를 설정하는데 제약이 발생할 수 있다(Humphries et al., 2002).
결과적으로 붉은박쥐 개체군 유지와 서식지 보전을 위해서는 동면기 정보만으로는 충분하지 않으며, 활동기 행동권 크기, 이동 패턴, 그리고 주요 자원의 공간적 배치를 파악하는 것이 필수적이라고 할 수 있다. 따라서 본 연구는 동면생태 중심으로 축적된 기존 연구의 한계를 보완하고, 붉은박쥐의 장기적 개체군 보호를 위한 과학적 기반을 확보하기 위해 활동기 행동권 크기와 서식지 환경특성을 정량적으로 규명하고자 수행하였다.
2. 재료 및 방법
2.1. 연구지역
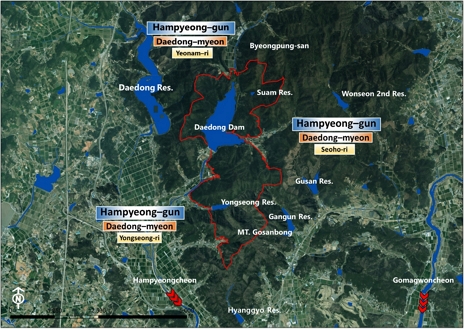
본 연구는 2025년 5월부터 10월까지 고산봉 붉은박쥐서식지 생태·경관보전지역을 중심으로 보전지역 내 위치한 주요 동면처와 주변 산림생태축 일원을 대상으로 수행되었다(Fig. 1). 고산봉 붉은박쥐서식지 생태·경관보전지역은 붉은박쥐 집단 동면처 확인에 따라 2002년 8,782 km2 일원이 생태·경관보전지역으로 지정·고시된 지역으로 2,700종 이상의 생물종과 38종의 멸종위기야생생물 및 희귀종(고유종, 보호종 등)이 서식하고 있다(NIE, 2023).
2.2. 개체포획
붉은박쥐 포획은 각성 직후 봄철, 수유 종료 후 여름철, 동면 전 가을철로 구분하여 수행하였다. 봄철 포획은 2025년 5월 말에서 6월 초 기간에 걸쳐 보호지역내 가장 많은 개체가 동면중인 2개소를 대상으로 하였으며, 각성 시기에 맞추어 포획장비(Mist-net, double-stacked mist net, mesh 16~32 mm, Shelves 4-5, USA; Harp-trap, BCM G5 Forest Strainer, USA)를 설치하여 출현하는 개체를 포획하였다. 여름철 활동기의 붉은박쥐 활동범위는 지금까지 구체적으로 알려진 바가 없으며, 동면처 주변이라고 규정할 수 없다. 따라서 여름철 포획은 봄철 파악된 행동권 범위를 포함하여 유사한 환경특성을 보이는 주변 산림축에 대하여 포획작업을 시도하였다. 가을철 포획은 봄철과 동일한 동면처를 대상으로 수행하였다. 일반적으로 붉은박쥐의 동면은 10월 중순부터 시작되는 것으로 알려져 있다. 그러나 본 연구에서 9월말 기존 동면처에 대한 확인결과 다수 개체의 동면처 귀소가 확인됨에 따라서 봄철과 동일한 장소 및 방법을 이용하여 포획하였다. 본 연구는 관련기관의 허가를 득한 후 이루어졌으며, 박쥐생태 전문가 및 수의사에 의한 개체 컨디션 점검 후 수행되었다.
2.3. VHF 발신기 및 GPS tag 부착
소형발신기(VHF transmitter) 부착을 통한 박쥐 행동권 연구는 가장 오래되고 널리 쓰이는 방법으로 본 연구에서는 부착 가능한 발신기 가운데 가장 소형 발신기(BD-2X, 0.28-0.35 g, 11.5×5.3×2.8 mm, LTM Single Stage Radio Transmitter)를 이용하였다. 발신기는 개체 무게대비 2.3%-3.4%로 설정하였으며, 부착은 견갑골 사이의 털을 제거한 후 의료용 접착제를 이용하여 부착하였다(Chung et al., 2010)(Fig. 2).

VHF and GPS transmitter deployment on Myotis rufoniger. From left to right: fur removal between the scapulae, attachment of a VHF transmitter and GPS tag.
지금까지 박쥐 행동권 파악을 위해 수행된 많은 연구에서는 고주파 신호 발신기(VHF)를 부착한 후 삼각측량 또는 연속추적을 통한 위치좌표 획득방법이 이용되었다. 그러나 이러한 방법에만 의존할 경우 연구자의 경험과 노하우에 따라 수집된 정보의 오차가 발생할 가능성이 있다(Bartolommei et al., 2012). 따라서 본 연구에서는 위성을 통해 위치좌표 수신이 가능한 GPS tag (Pinpoint-10, 1.0 g, Lotek Wireless, Canada)를 함께 이용하였으며, 연구에 이용된 tag 무게는 1.0 g 이하로 붉은박쥐의 무게 대비 7.0% 이내로 설정하였다(Fig. 2).
일반적으로 야생동물에 대한 발신기 부착은 5% rule을 적용하여 이루어지는 경우가 많다(Aldridge and Brigham, 1988). 그러나 박쥐 연구의 경우 발신기의 수명 및 GPS 기능을 고려할 때 기존의 rule은 적용하기 어려우며(Safi et al., 2007), 최근 박쥐를 대상으로 한 연구에 따르면 발신기의 무게 비율이 10%를 초과하는 경우에도 비행 행동이나 무게에 대한 기타 부정적 영향은 크지 않은 것으로 보고된 바 있다(Fujioka et al., 2020). Tag 부착은 재포획이 이루어지지 않거나 장기 부착에 따른 부정적 영향을 최소화 하기 위하여 용해성 봉합사(absorbable sutures)를 이용한 피부결속 방법을 적용하였다(Castle et al., 2015).
2.4. 원격무선추적
원격무선추적은 발신기에서 나오는 신호를 수신기를 통해 확인 후 연구자가 추적하는 방식으로 수신음에 대한 연속적인 추적 또는 삼각측량을 통한 위치확보 방법으로 이루어진다. 본 연구에서는 R2000 Receiver (ATS reveiver, Advanced Telemetry Systems, Inc., Isanti, MN), TRX 48S Receiver (48 channels, 148-222 MHz frequency range, Wildlife Materials International Inc. Canada), TRX 1000S Receiver (Standard band 173-174 MHz frequency range, Wildlife Materials International Inc., Canada), R20 Receiver (ICOM IC-R20 receiver, 150 kHz-3305 MHz), Biotracker VHF Receiver (Frequency range: 138-174 MHz, Gain control range: 90 dB, Fine funing: 1 kHz or 0.1 kHz steps, Loeck) 및 휴대용 3소자 Yagi 안테나(Hand-held three element Yagi Antenna)를 이용하였다.
야간 위치추적은 일몰 후부터 일출 전까지 수행하였으며, 최소 5명 이상의 숙련된 연구자가 동시에 참여하여 신호를 추적하였다. 연구자들은 서로 다른 지점에 배치되어 개체로부터 수신되는 신호의 방위각을 동시에 확보하였고, 삼각측량을 통해 위치좌표를 산출함으로써 추적 오차를 최소화하였다. 삼각측량이 어려운 경우에는 신호 강도 변화와 이동 방향을 지속적으로 확인하는 연속 추적 방식을 병행하여 개체의 이동 경로를 추적하였다. 야간 추적 과정에서 개체에 대한 위치좌표는 일정 시간 간격을 두고 반복적으로 확보하였으며, 각 위치 정보는 복수 연구자의 교차 확인을 거쳐 기록하였다. 연구자 간 숙련도 차이에 따른 위치 추정 편향을 최소화하기 위하여 조사 전 장비 운용 방법과 신호 해석 기준을 통일하였으며, 추적 과정 전반에서 동일한 절차와 판단 기준을 적용하였다.
2.5. 행동권 및 서식지 환경 분석
붉은박쥐 행동권 분석을 위하여 ArcGIS 10.1 (ESRI Inc.)의 homerange tool을 이용하였다. 위치추적을 통해 확보한 위치자료는 정확도 증대를 위하여 GPS 오차를 고려한 공간필터링을 실시하였으며, 분석 전 동일 좌표계로 변환하여 공간 적합성을 확보하였다. 붉은박쥐 행동권 분석은 위치좌표 최외각 점들을 연결하는 MCP (Minimum Convex Polygon) 100% 분석으로 수행하였다.
일반적으로 행동권 분석과정에서 Kernel Density Estimation (KDE) 50%를 핵심지역으로 분류하는데 이는 박쥐의 주요 채식지 범위와도 일치하며, 야간 비행활동 중 가장 중요한 핵심서식지(core area)로 표현할 수 있다(Laver and Kelly, 2008). 또한, KDE 분석은 위치자료가 불규칙하거나 불연속적으로 분포하는 경우에도 공간 분포를 추정할 수 있다는 장점이 있어, 비행 특성상 이동성이 높은 박쥐의 핵심서식지를 파악하는데 이용될 수 있다. 따라서 본 연구에서는 KDE 50%를 핵심서식지 분류 기준으로 설정하였다(Wilson et al., 2010).
지형자료는 국토지리정보원에서 제공하는 1:5,000 축척의 연속수치지도를 이용하여 수치표고모델(DEM, Digital Elevation Model)을 구축하였다. DEM 생성은 등고선 레이어를 추출한 후 TIN (Triangulated Irregular Network) 변환을 통해 수행하였으며, 분석용 raster는 1×1 m의 동일 격자(cell) 해상도로 변환하였다. 행동권 내 경관유형은 환경공간정보서비스에서 제공하는 세분류 토지피복도를 이용하여 분석하였다. 토지피복도는 대분류 체계에 따라 시가화·건조지역, 농업지역, 산림지역, 초지, 습지, 나지, 수역 등 7개 유형으로 구분하였다(Table 1).
3. 결 과
3.1. 붉은박쥐 행동권 크기
붉은박쥐 행동권 및 서식지 이용특성 파악을 위하여 2025년 5월부터 10월까지 총 19개체를 대상으로 수행하였다. 이용된 개체의 성별 및 연령 구성은 암컷 11개체 수컷 8개체이며, 여름철 포획된 수컷 아성체 1개체를 제외한 18개체는 모두 성체를 이용하였다. VHF 발신기는 총 15개체(F8, M7)에 부착하였으며, 나머지 4개체(F3, M1)에 대해서는 GPS tag를 부착하였다. 그러나 GPS tag 부착 개체의 경우 총 4개체 가운데 3개체는 tag 회수가 이루어지지 않았으며, 가을철 동면처로의 귀소 후 활동중인 1개체에 대해서만 회수가 이루어졌다.
총 19개체 가운데 위치추적 및 GPS 자료가 확보된 16개체에 대한 행동권 분석결과 붉은박쥐의 평균 행동권은 5.68±5.35 km2 (0.64 km2-18.38 km2)로 확인되었으며, 보전지역을 기준으로 이동거리는 평균 4.94 km (1.82 km-11.96 km)로 분석되었다(Table 2). 지금까지 국내 붉은박쥐의 활동기 서식지 이용에 대한 연구는 거의 이루어지지 않았으며, 짧은 활동기간을 감안할 때 동면처 주변에서 활동기를 보낼 것이라는 예측만 있을 뿐이었다(NIE, 2023). 그러나 본 조사결과 붉은박쥐의 행동권은 평균 5.68 km2, 최대 18.38 km2 이상의 행동권을 가지는 것으로 확인되었으며, 이동거리 또한 최대 11.96 km로 지금까지 국내에서 수행된 관박쥐 Rhinolophus ferrumequinum 0.69 km2 (Jeon et al., 2018), 대륙쇠큰수염박쥐 Myotis aurascens 0.17 km2 (Chung et al., 2013), 집박쥐 Pipistrellus abramus 0.15 km2 (Chung et al., 2010)와 비교할 때 상대적으로 큰 것으로 분석되었다.
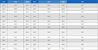
Individual characteristics and home range metrics of Myotis rufoniger obtained from radio-tracking and GPS data
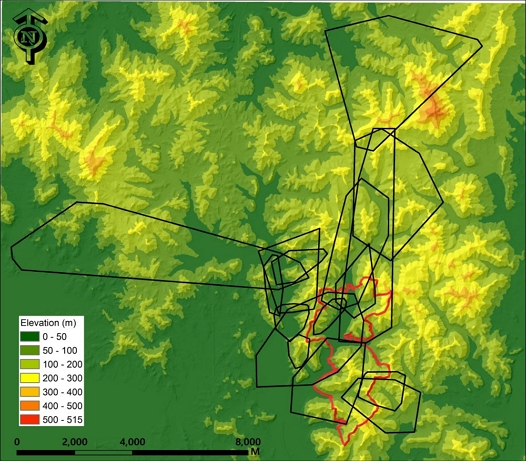
연구에 이용된 모든 개체는 보전지역 내부 뿐만 아니라 외부의 주변 서식지를 주요 행동권으로 이용하는 것으로 나타났으며, 보전지역 외부와 비교하여 내부에 대한 이용률은 낮은 것으로 분석되었다(Fig. 3). 생태경관보전지역 내부 이용률 분석결과 총 16개체 가운데 18.8% (3개체)만이 행동권의 50% 이상을 보전지역 범위에서 활동하였으며, 나머지 81.2% (13개체)의 경우 행동권 범위내 보전지역 이용률은 최소 0%에서 최대 38%로 나타났다.
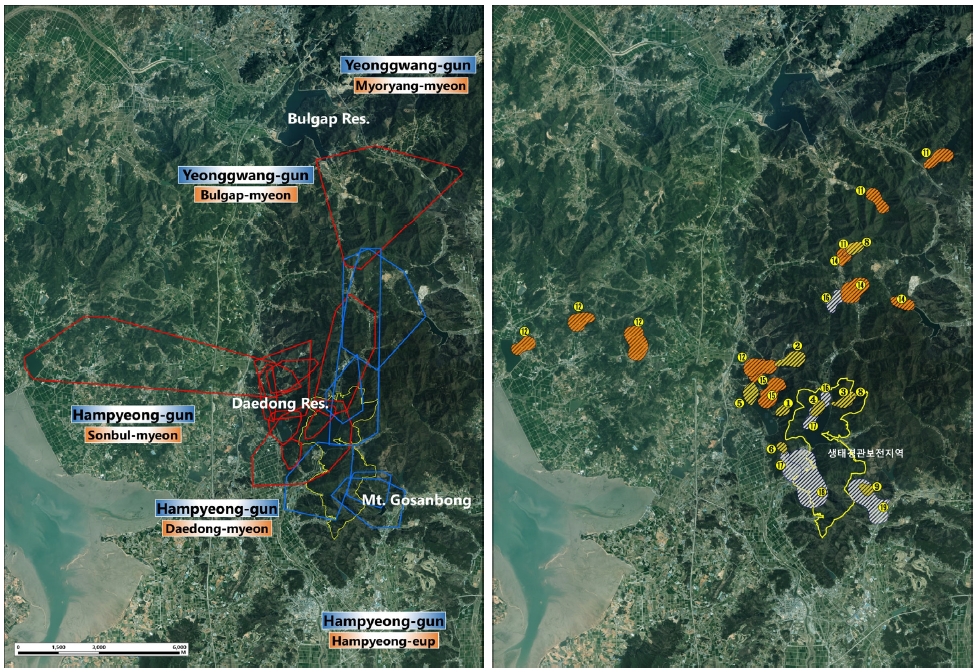
Home range extent (left) and core habitat locations (right) of Myotis rufoniger. In the home range map, red lines represent females, and blue lines represent males. The numbers assigned to core habitat locations indicate individual IDs.
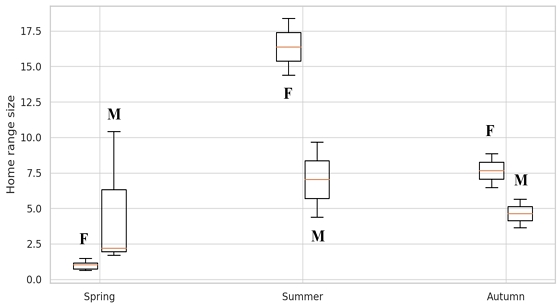
성별 및 계절에 따른 행동권 분석결과 붉은박쥐의 행동권은 여름철이 11.71±6.04 km2 (4.39 km2–18.38 km2)로 가장 큰 것으로 나타났으며, 다음으로 가을 6.15±2.16 km2 (3.64 km2–8.85 km2), 봄 2.42±3.27 km2 (0.64 km2–10.42 km2) 순으로 확인되었다. 계절에 따른 행동권 차이는 성별에 따라서도 명확한 차이를 보였는데 봄철의 경우 수컷의 행동권이 암컷보다 더 큰 경향을 보였으나, 여름철과 가을철은 암컷의 행동권이 더 큰 것으로 나타났다(Fig. 4). 특히 여름철의 경우 암컷의 행동권은 평균 16.39 km2로 수컷 7.03 km2과 비교하여 크게 증가하는 것으로 분석되었다. 암컷은 봄철(각성 직후) 평균 1.01±0.34 km2, 여름(수유 종료기) 평균 16.39±2.81 km2, 가을(번식기 종료 및 동면 전) 평균 7.67±1.68 km2로 계절에 따른 행동권 크기가 유의적으로 차이를 보인 반면(F=92.77, p<0.001), 수컷은 봄, 여름, 가을 각각 4.78±4.89 km2, 7.03±3.73 km2, 4.64±1.41 km2로 여름철 행동권이 가장 큰 것으로 나타났으나 계절별로 차이를 보이지는 않았다(F=0.32, p>0.05)(Table 3).
행동권 분석에 이용된 총 16개체에 대한 핵심서식지(채식지) 분석결과 평균 0.81±0.73 km2 (0.12 km2-2.31 km2)로 확인되었다(Table 2). 이는 붉은박쥐의 전체 행동권 평균 5.68 km2과 비교할 때 약 18.4%에 해당하는 것으로, 개체별로는 최소 4.7%에서 최대 40.2%를 차지하였다. 성별 및 계절에 따른 핵심서식지 비교결과 성별에 따른 유의성은 확인되지 않았다(F=0.840, p>0.05). 반면 계절에 따른 크기는 차이를 보였는데 암컷은 여름철이 가장 크고 수컷은 가을철이 가장 큰 것으로 나타났다(F=10.642, p<0.01). 본 연구에서 확인된 핵심지의 갯수는 평균 1.7개로(최소 1개-최대 4개) 여름철 평균 3.0개, 가을철 평균 1.5개, 봄철 평균 1.1개 순으로 나타났으며, 핵심서식지의 개수는 행동권 크기가 커질수록 증가하는 경향을 보였다(Fig. 3).
분석된 전체 개체의 핵심서식지 중첩결과 다수의 개체에서 핵심지역 중첩이 확인되었으며, 일부 지역에서는 최대 3개체의 핵심서식지가 중첩되는 것으로 분석되었다. 개체별 핵심서식지의 중첩 비율은 적게는 10% 미만에서 많게는 80% 이상으로 나타났으며, 이러한 핵심지역 중첩 지역은 주로 산림 가장자리에 위치한 저수시설(저수지, 연못)이나 계곡부가 포함된 지역에 집중되는 경향을 보였다.
3.2. 붉은박쥐 서식지 환경특성
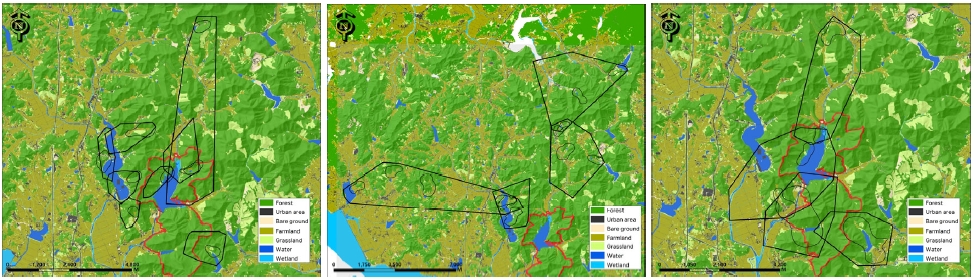
붉은박쥐의 행동권 범위내 평균 고도는 160 m 이하로 분석되었으며, 60% 이상은 200 m 이하로 나타났다. 계절별로는 여름철이 가장 높고 가을철이 가장 낮은 고도범위를 보였으며, 사면향은 뚜렷한 경향성 없이 다수의 개체가 평지지역에 대한 이용률이 높은 것으로 나타났다(Fig. 5). 경사도는 평균 11.9-25.2°범위로 비교적 낮은 경사도를 선호하는 경향을 보였으며, 토지이용 유형은 일부 각성 직후 개체에서 동면처 주변 수계에 대한 높은 이용률을 보이기도 했으나 전체 개체로 볼 때 산림지역, 수역(저수지, 하천), 경작지 순의 비율을 보였다. 붉은박쥐에 대한 종합적인 환경특성 분석 결과, 성별에 대한 서식지 선호유형은 확인되지 않았지만, 시기에 따라서 암수 모두 수계 서식지, 산림내 계곡부, 산림 가장자리, 임연부 초지 및 경작지에 대한 이용률이 높은 것으로 확인되었다(Table 4).
핵심서식지 환경특성 분석결과, 고도 20-279 m 범위의 저지대를 중심으로 이용하는 것으로 나타났으며, 평균 경사도는 대부분 20°미만으로 비교적 완만한 지역을 선호하는 것으로 분석되었다. 암수 모두 사면향에 대한 경향성은 보이지 않았으며, 봄철과 가을철 기간내 일부 개체의 평지지역 선호도가 높게 나타났다. 핵심서식지에 대한 임상구조는 활엽수림의 비율이 가장 높은 것으로 분석되었다(Table 5).
결과적으로 붉은박쥐의 야간 핵심서식지(채식지) 이용은 산림내·외부에 위치한 저수지 또는 주변지역을 중심으로 이루어지는 것으로 확인되었으며, 동시에 산림 가장자리에 대한 이용률이 높은 것으로 나타났다. 이러한 저수지(수계)와 산림 가장자리 지역에 대한 채식지 의존성은 성별과 관련없이 유사한 패턴을 보였으며, 특히 행동권 크기가 상대적으로 작은 봄철과 가을철에 집중되는 것으로 나타났다(Fig. 6).
4. 고 찰
4.1. 붉은박쥐 행동권 및 서식지 환경
붉은박쥐 행동권 분석결과 평균 행동권은 5.68±5.35 km2, 최대 행동권은 18.38 km2로 나타났다. 이러한 결과는 지금까지 붉은박쥐의 공간이용 정보가 없던 상황에서 짧은 활동기 동안 동면처 주변을 제한적으로 이용할 것이라는 예상과 상반된다고 할 수 있으며(NIE, 2023), 개체별 에너지 요구량, 곤충 발생의 시·공간 변동, 산림 구조의 이질성, 경관 연결성 등 다양한 환경 요인이 행동권 범위와 밀접한 관련이 있음을 보여주는 결과이다. 특히, 표준편차가 5.35 km2로 나타난 결과는 개체간 행동권 크기의 변동폭이 매우 크다는 것을 보여주며, 이는 서식환경의 이질성 및 개체별 생리·행동 특성 차이가 크게 작용했음을 시사한다. 이러한 행동권 특성은 본 연구에서 나타난 최대 11.96 km 장거리 이동이 뒷받침하고 있으며, 붉은박쥐의 생태적 요구는 동면처 주변의 보전지역 공간범위를 넘어선다는 것을 말해준다. 따라서 행동권 크기의 높은 변동성을 고려할 때 붉은박쥐 보호활동시 평균 행동권 크기로 접근하는 것은 부적절할 수 있으며, 행동권 외곽부 및 이동경로까지 고려한 기능적 서식지 연결성 확보가 필요하다고 할 수 있다.
산림 가장자리, 수계, 농경지 주변은 곤충 밀도가 높고 비행 경로 안정성이 확보되는 지역으로, 많은 박쥐류가 핵심 채식지로 활용한다(Kunz et al., 2011). 본 연구에서도 이러한 서식지 유형에서 중첩율이 높았으며, 이는 붉은박쥐의 채식지 선택은 공간적 경관유형에 따라 다양하게 이용된 결과라고 할 수 있다. 본 연구의 핵심서식지(KDE 50%) 크기는 평균 0.81±0.73 km2로, 전체 행동권의 약 18.4%에 해당하며, 이용하는 핵심지의 개수는 평균 1.7개로 나타났다. 이처럼 적은 개수와 특정 지점에 대한 핵심지 이용은 식충성 박쥐가 넓은 행동권 내에서도 실제 채식 효율이 높은 한정된 지역을 반복적으로 이용한다는 기존 연구와 일치하는 것으로(Boyles et al., 2007), 본 연구에서 핵심지 환경으로 도출된 산림 가장자리와 저수지 주변의 경관구조는 다른 서식지 유형과 비교하여 효율적인 먹이원 확보가 가능한 지점이라고 예측할 수 있다.
붉은박쥐 성별에 따른 행동권 크기 및 계절별 변화는 암수의 생리생태적 특징을 대변하는 것으로 판단된다. 암컷의 행동권은 여름철이 평균 16.39 km2로 가장 크고 다음으로 가을철 평균 7.67 km2, 봄철 평균 1.01 km2 순으로 나타났다. 봄철 각성 직후 출현한 암컷 개체의 경우 대사활동을 위한 에너지 소모량과 비교하여 체내 지방축적량이 매우 낮은 상태일 뿐 아니라(Jonasson and Willis, 2012) 제한된 시간내 배란·임신·출산을 성공시켜야하는 생리적 부담 상태로 볼 수 있다. 따라서 이 시기의 붉은박쥐는 에너지 소모 최소화 전략을 이용한 것으로 해석할 수 있으며, 최소화 방법으로 장거리 비행 및 원거리 채식지 선택 대신 동면처 주변의 제한된 서식지를 이용한 결과로 판단된다.
본 연구의 여름철 조사는 암컷의 번식활동이 종료된 7월 말-8월 초 수행된 것으로 이 시기의 암컷은 수유에 대한 스트레스가 없는 반면, 체내 에너지 요구량은 상대적으로 높다고 할 수 있다(Racey and Speakman, 1987). 따라서 새끼에 대한 양육이 끝난 암컷의 경우 양질의 먹이원 확보를 통한 지방축적을 위해 긴 시간의 야간비행과 보다 먼 거리까지의 채식지 이용이 이루어진다(Kurta et al., 1989). 뿐만 아니라 스스로 자율비행이 가능한 어린 개체와의 채식지 중첩을 피하는 전략 또한 행동권 확장의 원인 가운데 하나로 판단된다.
동면 전 수행된 가을 조사의 경우 비록 여름철과 비교하면 작은 행동권을 보였으나, 각성 직후인 봄철과 비교하면 큰 것으로 나타났다. 일반적으로 온대성 박쥐의 가을(동면 전)은 지방 축적을 극대화하는 시기로 먹이원의 양적·질적 탐색 범위를 확장하는 시기로 볼 수 있다(Ransome, 1990; McGuire et al., 2014). 특히 붉은박쥐와 같은 큰수염박쥐속(Myotis)의 경우 곤충 밀도가 점차 낮아지는 여건에서 효율적인 먹이원 확보를 위한 행동권 확장 경향이 두드러진다(Divoll et al., 2022). 그러나 이러한 확장 필요성에도 불구하고 여름철과 비교하여 상대적으로 작은 행동권이 나타난 이유는 붉은박쥐의 경우 기타 동굴성 박쥐와 비교하여 동면 시작점이 상대적으로 빠르며(Chung, 2020), 본 조사가 이루어진 가을철의 경우 먹이원 확보를 통한 지방축적보다 동면 시기가 임박한 시점에 이루어진 결과로 판단된다.
수컷의 경우 암컷과 동일하게 여름철 행동권이 가장 큰 것으로 나타났으나, 암컷과 비교하여 계절별 차이는 크지 않은 것으로 확인되었다. 수컷 박쥐는 번식에 대한 스트레스가 없는 상태로 연중 에너지 효율성 극대화 전략을 이용한다(Kerth, 2008; Dorrestein et al., 2024). 따라서 암컷의 번식기 동안에도 기상상황에 따라서 일시적 지둔상태에 들기도 하며(Komar et al., 2020), 먹이원의 풍부도에 따라 일정한 변화패턴 없이 다양한 지역에서 채식활동을 하는데 이러한 수컷의 생리생태적 특징으로 인하여 계절별 행동권 변화폭은 암컷과 비교하여 적은 것으로 판단된다. 그러나 비록 계절별 유의적 차이는 나타나지 않았으나 수컷의 여름철 행동권은 봄, 가을과 비교하여 상대적으로 큰 것으로 나타났는데 이러한 경향성은 먹이원의 풍부도에 따라 행동권 및 채식지 선택의 다양성이 높아졌기 때문으로 판단된다. 일반적으로 수컷의 경우 교미를 위한 암컷 탐색 및 동면 전 지방축적을 위한 먹이활동 증가에 따라 가을철에 행동권이 큰 경향을 보인다(Fraser and McGuire, 2023). 그러나 본 연구가 이루어진 시기는 붉은박쥐의 동면이 임박한 시점임을 고려할 때 가을철 확장된 행동권을 대변한다고 볼 수 없으며, 이에 대한 부분은 향후 추가적으로 연구되어야 할 것으로 판단된다.
일반적으로 산림성 박쥐의 임상 선호도는 곤충 밀도가 높은 활엽수림을 선호하는 것으로 알려져 있으나(Catto et al., 1996; Mackie and Racey, 2007), 본 연구결과 일부 개체의 경우 핵심서식지 범위내 침엽수림 비율이 상대적으로 높은 것으로 분석되었다. 이러한 결과는 암컷 개체의 봄철 각성 직후 에너지 소모 최소화를 위해 동면지 인근에 대한 높은 이용률을 포함하여 침엽수림과 인접한 산림 가장자리, 수계, 경작지 등을 이용한 결과에 기인한 것이다. 따라서 이는 침엽수림에 대한 높은 비율로 해석하기보다 산림 가장자리 경관 유형에 따른 결과로 이해되어야 한다.
붉은박쥐의 행동권 이용은 해발 160 m 이하의 저지대와 낮은 경사도 지역을 중심으로 확인되었다. 토지이용 비율은 산림지역이 가장 높게 나타났으나 개체 및 계절에 따라서 산림 가장자리에 조성된 경작지와 다양한 형태의 수계 서식지를 선호하는 것으로 확인되었으며, 특히 행동권 크기가 작은 봄철과 가을철에 이러한 경향이 두드러지는 것으로 나타났다.
박쥐의 야간 채식지 이용과 선호도는 저수지, 운하, 연못, 계곡 등과 같은 수계 서식지와(Zukal and Rehak, 2006; Chung et al., 2015; Jeon et al., 2023) 산림 가장자리를 중심으로 높게 나타나며, 이러한 서식지 이용은 번식상태와 계절에 따라서 변화하는 경향을 보인다(Robinson and Stebbings, 1997). 이는 수계 서식지의 경우 수면위를 포함하여 수변 식생 주변으로 곤충의 풍부도가 높기 때문이며(Zukal and Rehak, 2006), 산림 가장자리는 곤충의 밀도가 높을 뿐만 아니라 복합적인 서식지 구조와 비교하여 안정적인 비행존을 유지시켜주기 때문으로 알려져 있다(Verboom and Huitema, 1997). 또한 수계 서식지는 상대적으로 기온이 낮은 봄과 가을 시기에도 먹이자원 확보가 용이한 특징이 있으며, 그에 따라 암컷의 경우 에너지 요구량이 많은 계절에 수계 주변에서의 비행활동 빈도가 높은 경향을 보인다(Bartonicka and Rehak, 2004). 이러한 선행 연구결과 및 본 연구에서 나타난 채식지 이용특성을 고려할 때 수계 및 산림 가장자리 서식지는 붉은박쥐의 핵심서식지 기능을 한다고 볼 수 있으며, 특히 에너지 요구량이 증가하는 봄철과 가을 시기에 대한 수계 의존성은 이러한 서식지 중요성을 반증하는 결과로 판단된다.
이러한 에너지 효율성 전략 외에도 붉은박쥐의 저지대 및 산림 가장자리와 수계지역에 대한 서식지 이용 특성은 본 연구대상지역의 지형적 특성 또한 무관하지 않은 것으로 판단된다. 본 연구가 이루어진 지역의 경우 주변 15 ㎞ 범위의 최고 해발고도는 400 m 이하로 붉은박쥐 개체별 행동권 범위를 고려할 때 경관 유형은 다양하게 조성되어 있는 반면 서식지별 고도차는 크지 않다. 또한 산림 가장자리로는 많은 면적의 경작지가 조성되어 있으며, 이와 관련된 저수시설(저수지, 댐, 소류지 등) 또한 산재해 있다. 따라서 붉은박쥐의 서식지 환경특성과 관련하여 저지대 산림 가장자리 및 수계 의존성에 대한 부분은 향후 연구대상지 확대를 통한 비교가 이루어져야 할 것으로 판단된다.
4.2. 연구의 한계 및 추가 연구제언
비행하는 박쥐에 대한 행동권 연구는 많은 개체수와 다양한 시기에 걸친 지속적인 연구가 이루어져야 한다(O'Mara et al., 2014). 최근에 수행된 박쥐 행동권 연구의 경우 많은 양의 샘플과 다양한 추적방법이 이용되고 있는데, True et al.(2023)은 Eastern red bat (Lasiurus borealis)의 행동권 연구를 위해서 총 115개체를 이용하였으며, Lagerveld et al.(2024)은 Nathusius pipistrelle (Pipistrellus nathusii)를 대상으로 총 44개체를 이용하여 원격무선추적을 수행하였다. 또한 McCracken et al.(2016)은 박쥐의 장거리 이동에 대한 위치자료 누락을 최소화하기 위하여 항공기를 이용한 추적을 수행하였다.
그러나 본 연구에서는 16개체의 적은 개체수와 계절별 단기간의 조사로 수행되었으며, 추적방법 또한 차량과 도보를 이용함에 따라 비행을 통하여 야간에 이동하는 박쥐의 위치정보에 누락 가능성을 배제할 수 없다. 따라서 본 연구에서 확인된 붉은박쥐의 행동권 크기는 개체별 최소 크기로 해석되어야 하며, 학술자료 및 환경영향평가 활용시 보다 원거리로의 이동 가능성이 고려되어야 한다.
식충성 박쥐는 계절과 먹이원의 풍부도에 따라 다양한 서식지를 이용하며, 이러한 과정에서 보다 높은 고도와 산림내 특정 환경에 대한 이용률이 높아질 수 있다(Gonsalves et al., 2013). 그러나 본 연구에서는 붉은박쥐 행동권 면적의 60% 이상이 해발 200 m 이하로 산출되었으며, 이러한 결과는 본 연구가 이루어진 지리적 특성과도 무관하지 않을 것으로 판단된다. 본 연구가 이루어진 보전지역은 저수지, 경작지, 민가, 산림이 모두 연결된 곳으로 반경 15 km내 고도는 평균 400 m 이하로 낮은 특징을 보인다. 따라서 본 연구에서 나타난 서식지 이용특성은 붉은박쥐의 에너지 효율성 증대를 위한 채식지 선택 전략으로 해석할 수 있으나, 지리적 환경특성 또한 배제할 수 없다. 따라서 장기적인 붉은박쥐 개체군 보호 및 서식지 관리를 위해서는 지속적인 행동권 추가연구를 통하여 본 결과에 대한 정량적 보완이 이루어져야 하며, 연구대상지 다변화를 통한 종 고유의 특이성 및 경관 유형에 따른 변화상 파악이 연계되어야 할 것으로 판단된다.
5. 결 론
본 연구는 국내에서 최초로 붉은박쥐(Myotis rufoniger)의 활동기 행동권과 핵심서식지의 공간적 특성을 정량적으로 규명하였다는 점에서 중요한 의의를 갖는다. 지금까지 붉은박쥐 생태 연구는 대부분 동면처의 미기후 및 동면 패턴에 초점을 두어 수행되어 왔으며, 활동기 공간이용 특성에 관한 연구는 거의 이루어지지 않았다. 그러나 붉은박쥐 보전전략 수립을 위해서는 동면기뿐 아니라 활동기의 행동권 크기 및 서식지 이용특성을 이해하는 것이 필수적이며, 본 연구는 이러한 생태정보의 공백을 보완할 수 있는 자료이다. 본 연구는 붉은박쥐 보전전략 수립과 관련해서 보전지역 외부의 산림 가장자리 및 수계 서식지의 중요성에 대한 확인과 함께 동면처 중심의 보전활동에서 벗어나 경관 연결성 확보 및 외부 핵심서식지 보호와 같은 보전지역 외부 경관구조를 함께 고려한 서식지 관리가 필요하다는 것을 보여준다.
Acknowledgments
본 연구는 「붉은박쥐 행동권 및 서식지 특성 연구」사업의 지원을 받아 수행되었음.
REFERENCES
-
Aldridge, H., Brigham, R., 1988, Load carrying and maneuverability in an insectivorous bat: a test of the 5% “rule” of radio-telemetry, J. Mammal., 69, 379-382.
[https://doi.org/10.2307/1381393]

- Bartolommei, P., Francucci, S., Pezzo, F., 2012, Accuracy of conventional radio telemetry estimates: a practical procedure of measurement, Hystrix, 23, 12-18.
-
Bartonicka, T., Rehak, Z., 2004, Flight activity and habitat use of Pipistrellus pygmaeus in a floodplain forest, Mammalia, 68, 365-375.
[https://doi.org/10.1515/mamm.2004.036]

-
Boyles, J. G., Dunbar, M. B., Stom, J. J., Brack Jr, V., 2007, Energy availability influences microclimate selection of hibernating bats, J. Exp. Biol., 210, 4345-4350.
[https://doi.org/10.1242/jeb.007294]

-
Castle, K. T., Weller, T. J., Cryan, P. M., Hein, C. D., Schirmacher, M. R., 2015, Using sutures to attach miniature tracking tags to small bats for multi-month movement and behavioral studies, Ecol. Evol., 5, 2980-2989.
[https://doi.org/10.1002/ece3.1584]

-
Catto, C. M. C., Hutson, A. M., Racey, P. A., Stephenson, P. J., 1996, Foraging behaviour and habitat use of the serotine bat (Eptesicus serotinus) in southern England, J. Zool. Lond., 238, 623-633.
[https://doi.org/10.1111/j.1469-7998.1996.tb05419.x]

- Chung, C. U., Han, S. H., Lee, C. I., 2010, Home-range analysis of Pipistrellus abramus in non-reproductive season using radio-tracking, Kor. J. Env. Eco., 24, 487-492.
- Chung, C. U., Han, S. H., Kim, S. D., Lim, C. W., Kim, S. C., Kim, C. Y., Lee, H. J., Kwon, Y. H., Kim, Y. C., Lee, C. I., 2011, Home-ranges of female Pipistrellus abramus in different reproductive stages revealed by radio-telemetry, Kor. J. Env. Eco., 25, 001-009.
-
Chung, C. U., Kim, S. C., Han, S. H., 2013, Diurnal roost selection and home range size in Myotis aurascens, J. Env. Sci. Int., 22, 1227-1234.
[https://doi.org/10.5322/JESI.2013.22.9.1227]

-
Chung, C. U., Han, S. H., Cha, J. Y., Kim, S. C., Kim, J. J., Jeong, J. C., Lim, C. W., 2015, The diet composition of the serotine bat Eptesicus serotinus revealed by faecal analysis, Kor. J. Env. Eco., 29, 368-373.
[https://doi.org/10.13047/KJEE.2015.29.3.368]

- Chung, C. U., 2020, A Field guide to Korean bats, Econature Press, Seoul, 1-272.
-
Dorrestein, A., Westcott, D., Martin, J. M., Phalen, D., Rose, K., Welbergen, J. A., 2024, Bat mating systems-A Review and recategorisation, Ecol. Evol., 14, 1-21.
[https://doi.org/10.1002/ece3.70149]

-
Divoll, T. J., Aldrich, S. P., Haulton, G. S., O'Keefe, J. M., 2022, Endangered Myotis bats forage in regeneration openings in a managed forest, Fore. Ecol. Manage., 503, 119757.
[https://doi.org/10.1016/j.foreco.2021.119757]

-
Fenton, M. B., 1970, A Technique for monitoring bat activity with results obtained from different environments in southern Ontario, Can. J. Zool., 48, 847-851.
[https://doi.org/10.1139/z70-148]

- Fenton, M. B., Simmons, N. B., 2014, Bats: Phylogeny and Evolution, University of Chicago Press, 1-240.
-
Fraser, E. E., McGuire, L. P., 2023, Prehibernation swarming in temperate bats, Can. J. Zool., 101, 408-422.
[https://doi.org/10.1139/cjz-2022-0129]

-
Fujioka, E., Yoshimura, K., Ujino, T., Yoda, K., Fukui, D., Hiryu, S., 2020, Foraging and commuting habitats of the greater horseshoe bat revealed by high-resolution GPS tracking, Research Square, 1-18.
[https://doi.org/10.21203/rs.3.rs-26350/v1]

-
Gonsalves, L., Law, B., Webb, C., Monamy, V., 2013, Foraging ranges of insectivorous bats shift relative to changes in mosquito abundance, PLoS ONE, 8, 1-10.
[https://doi.org/10.1371/journal.pone.0077183]

-
Henry, M., Thomas, D. W., Vaudry, R., Carrier, D., 2002, Foraging distances and home range of pregnant and lactating little brown bats, J. Mammal., 83, 767-774.
[https://doi.org/10.1644/1545-1542(2002)083<0767:FDAHRO>2.0.CO;2]

-
Humphries, M. M., Thomas, D. W., Speakman, J. R., 2002, Climate-mediated energetic constraints on the distribution of hibernating mammals, Nature, 418, 313-316.
[https://doi.org/10.1038/nature00828]

-
Jeon, Y. S., Kim, S. C., Han, S. H., Chung, C. U., 2018, Characteristics of the home range and habitat use of Rhinolophus ferrumequinum in an urban landscape, J. Env. Sci. Int., 27, 665-675.
[https://doi.org/10.5322/JESI.2018.27.8.665]

-
Jeon, Y. S., Kim, S. C., Lim, C. W., Chung, C. U., 2023, Habitat use characteristics and the possibility of bats as indicator species of farming methods, J. Env. Sci. Int., 32, 685-692.
[https://doi.org/10.5322/JESI.2023.32.10.685]

-
Jonasson, K. A., Willis, C. K. R., 2012, Hibernation energetics of free-ranging little brown bats, J. Exp. Biol., 215, 2141-2149.
[https://doi.org/10.1242/jeb.066514]

-
Kerth, G., 2008, Causes and consequences of sociality in bats, BioScience, 58, 737-746.
[https://doi.org/10.1641/B580810]

-
Kim, S. S., Choi, Y. S., Kim, B. H., Yoo, J. C., 2009, The current distribution and habitat preferences of hibernating Myotis formosus in Korea, J. Ecol. Field Biol., 33, 191-195.
[https://doi.org/10.5141/JEFB.2009.32.3.191]

-
Komar, E., Dechmann, D. K. N., Fasel, N. J., Zegarek, M., Ruczyński, I., 2020, Food restriction delays seasonal sexual maturation but does not increase torpor use in male bats, J. Exp. Biol., 223, 1-9.
[https://doi.org/10.1242/jeb.214825]

-
Kunz, T. H., Braun de Torrez, E., Bauer, D., Lobova, T., Fleming, T. H., 2011, Ecosystem services provided by bats, Ann. N.Y. Acad. Sci., 1223, 1-38.
[https://doi.org/10.1111/j.1749-6632.2011.06004.x]

- Kunz, T. H., Reichard, J. D., 2010, Bat roosts in buildings: management and conservation, in: Mitchell-Jones, T., Richardson, P. (eds.), Springer, 151-176.
-
Kurta, A., Bell, G. P., Nagy, K. A., Kunz, T. H., 1989, Energetics of pregnancy and lactation in free-ranging little brown bats, Physiol. Zool., 62, 804-818.
[https://doi.org/10.1086/physzool.62.3.30157928]

-
Lagerveld, S., de Vries, P., Noort, B., Stienstra, K., Sonneveld, C., Vallina, T., Keur, M., Steenbergen, J., 2024, Coastal and offshore movements of Nathusius’pipistrelle during autumn migration, Wageningen Marine Res., 1-226.
[https://doi.org/10.18174/658603]

-
Laver, P. N., Kelly, M. J., 2008, A Critical review of home range studies, J. Wildl. Manage., 72, 290-298.
[https://doi.org/10.2193/2005-589]

-
Mackie, I. J., Racey, P. A., 2007, Habitat use varies with reproductive state in noctule bats, Biol. Conserv., 140, 70-77.
[https://doi.org/10.1016/j.biocon.2007.07.031]

-
McCracken, G. F., Safi, K., Kunz, T. H., Dechmann, D. K., Swartz, S. M., Wikelski, M., 2016, Airplane tracking documents the fastest flight speeds recorded for bats, R. Soc. Open Sci., 3, 160398.
[https://doi.org/10.1098/rsos.160398]

- McGuire, L. P., Fenton, M. B., Guglielmo, C. G., 2014, Phenotypic flexibility in migratory bats, J. Exp. Biol., 217, 882-892.
- Moore, P. R., 2016, Home range and habitat use of foraging gray bats (Myotis grisescens) from five maternity sites in northern Arkansas, Master’s thesis, Arkansas State University, 1-79.
- National Institute of Ecology (NIE), 2023, Detailed survey of ecological landscape conservation areas: Gosanbong habitat of Myotis rufoniger, Ministry of Environment, 1-873.
-
O’Mara, M. T., Wikelski, M., Dechmann, D. K. N., 2014, 50 years of bat tracking: Device attachment and future directions, Methods Ecol. Evol., 5, 311-319.
[https://doi.org/10.1111/2041-210X.12172]

- Racey, P. A., Speakman, J. R., 1987, The energy costs of pregnancy and lactation in heterothermic bats, Symp. Zool. Soc. Lond., 57, 107-125.
- Ransome, R. D., 1990, The natural history of hibernating bats, Christopher Helm, London, 145-170.
-
Robinson, M. F., Stebbings, R. E., 1997, Home range and habitat use by the serotine bat Eptesicus serotinus in England, J. Zool. Lond., 243, 117-136.
[https://doi.org/10.1111/j.1469-7998.1997.tb05759.x]

-
Roschewitz, I., Gabriel, D., Tscharntke, T., Thies, C., 2005, Landscape complexity effects on arable weed species diversity in organic vs. conventional farming, J. Appl. Ecol., 42, 873-882.
[https://doi.org/10.1111/j.1365-2664.2005.01072.x]

-
Safi, K., König, B., Kerth, G., 2007, Sex differences in population genetics, home range size, and habitat use of the parti-colored bat (Vespertilio murinus, Linnaeus 1758) in Switzerland and their consequences for conservation, Biol. Conserv., 137, 28-36.
[https://doi.org/10.1016/j.biocon.2007.01.011]

-
True, M. C., Goman, K. M., Taylor, H., Reynolds, R. J., Ford, W. M., 2023, Fall migration, oceanic movement, and site residency patterns of eastern red bats (Lasiurus borealis) on the mid-Atlantic Coast, Movement Ecol., 11, 35, 1-16.
[https://doi.org/10.1186/s40462-023-00398-x]

-
Verboom, B., Huitema, H., 1997, The importance of linear landscape elements for the pipistrelle Pipistrellus pipistrellus and the serotine bat, Landscape Ecol., 12, 117-125.
[https://doi.org/10.1007/BF02698211]

-
Wilson, R. R., Hooten, M. B., Strobel, B. N., Shivik, J. A., 2010, Accounting for individuals, uncertainty, and multiscale clustering in core area estimation, J. Wildl. Manage., 74, 1343-1352.
[https://doi.org/10.1111/j.1937-2817.2010.tb01256.x]

- Zukal, J., Rehak, Z., 2006, Flight activity and habitat preference of bats in a karstic area, Folia Zool., 55, 273-281.
- Yeongsan River Basin Environmental Office (YBEO), 2006, Status of red bat habitats along the southwestern coast, Ministry of Environment, Korea, 3-19.
Ecological Education Center, Dongguk Universitybatman424@naver.com
Division of Academic Research, Econet Co. Ltdbigboss369@naver.com
Division of Academic Research, Econet Co. Ltdbatman8122@gmail.com
Division of Academic Research, Econet Co. Ltdtlrqkd01@naver.com