철 담지 바닥재 기반 제올라이트를 이용한 반월시화산업단지 하천 내 비소 및 중금속 오염 퇴적물의 안정화 처리
Ⓒ The Korean Environmental Sciences Society. All rights reserved.
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Surface modification strategies for coal ash zeolites are required for the simultaneous and efficient treatment of both cationic and anionic pollutants. In this study, Fe was incorporated onto the surface of a bottom ash-based zeolite (Fe@BAZ), synthesized via the fusion method, as a potential amendment for the stabilization of sediment contaminated by As and heavy metals. According to the adsorption isotherm study, the maximum Fe@BAZ adsorption capacity of As(Ⅲ), As(Ⅴ), and Pb was found to be 38.76 mg/g, 47.95 mg/g, and 344.83 mg/g, respectively. To evaluate the stabilization performance of Fe@BAZ, cultivation experiments were conducted using contaminated sediment samples collected from a stream in the Banwol-Sihwa industrial complex. The mobility and toxicity reduction of contaminants (As, Cd, Pb, Cu, and Zn) in the sediments were assessed using TCLP and 1 M NH4NO3 leaching tests during the incubation period. Fe@BAZ is expected to be highly suitable as a multifunctional material that can utilize bottom ash discharged from thermal power plants as a high value added resource, reducing the risks associated with contaminated sediments destined for landfill.
Keywords:
Sediment, Arsenic, Heavy metal, Zeolite, Bottom ash, Stabilization1. 서 론
퇴적물은 여러 가지 물질이 혼합되어 수역의 밑바닥에 가라앉은 것을 말하며 저서 생물의 부산물(껍질 및 사체)과 지표로 부터 유입되는 유실 토양 입자, 유기물(식물체 및 동물의 사체 등), 하수, 산업 폐기물, 기타 유·무기 물질, 화학물질을 포함한다(USEPA, 1993). 하천에 유입되는 용존성 오염물질은 퇴적물에 흡착 및 결합되며 입자상 오염물질은 유속 및 하천 지형과 같은 수리학적 특성에 영향을 받으며 입자의 무게 순서로 유속이 감소되는 구간부터 서서히 퇴적된다(Dean, 2005; Yang, 2019).
Jeong et al.(2019)은 시화호 퇴적물의 오염기원을 연구하기 위해 반월시화산업단지를 관통하여 시화호로 유입되는 5개 하천에서 퇴적물을 채취하여 분석한 결과 Cu, Zn, Pb, Cd의 농도가 각각 2,549 mg/kg, 1,742 mg/kg, 808 mg/kg, 5.8 mg/kg으로 확인되었다(Jeong, 2019). 이러한 고농도 퇴적물의 경우 자원으로 활용하기 어려우며 오염 특성상 처리가 어렵고 효율이 떨어지기 때문에 준설 퇴적물은 주로 매립처리 되고 있다. 매립된 퇴적물 중 유해한 중금속은 침출수 등에 의해 외부로 유출 및 확산될 수 있기 때문에 오염 퇴적물 매립 시 중금속의 이동성 및 위해성을 저감시킬 수 있는 기술이 요구된다(Sun, 2020).
KEI(2014)의 연구에 따르면 연간 약 800만 톤의 석탄재가 발생되고 있으고 이 중 바닥재는 시멘트 또는 콘크리트 결합재의 성분이 적합성이 떨어지기 때문에 재활용률이 낮으며 새로운 재활용 방안 필요하다. 화력발전소에 발생되는 석탄재를 이용한 제올라이트의 합성은 폐기물을 고부가가치 자원으로 활용할 수 있으며 양이온 중금속에 높은 반응성을 가지고 있어 이를 이용한 여러 연구가 진행되어 왔다(Koshy, 2016). 그러나 비소와 같은 음이온성 오염물질에 대한 반응성은 낮기 때문에 비소와 중금속의 동시 처리를 위해서는 표면 개질이 필요하다(Angaru, 2022).
본 연구에서는 오염 퇴적물 중 비소 및 중금속의 위해성을 동시에 저감할 수 있는 철 개질 바닥재 기반 제올라이트(Fe-modified bottom ash based zeolite, Fe@BAZ)를 제조하였으며 특성평가, 수중 흡착실험, 배양실험을 통해 성능을 확인하고자 하였다. 또한 배양실험에서는 실제 반월시화산업단지에서 채취한 비소 및 중금속 오염된 퇴적물을 이용하여 개발한 소재의 현장 적용 가능성을 평가하고자 하였다.
2. 재료 및 방법
2.1. 철 개질 바닥재 기반 제올라이트 합성
바닥재 기반 제올라이트(Bottom ash based zeolite, BAZ)의 합성을 위해 한국서부발전의 태안발전본부의 회처리장에서 매립된 것을 채취하였으며 해당 바닥재는 보일러 하부에서 포집 후 분쇄된 것이다. 바닥재에는 잔존하고 있는 미연탄소분과 불순물이 존재하기 때문에 이를 제거하기 위해 입경의 크기가 2 mm이 되도록 체거름하고 1 M HCl 용액에서 세척한 후 800oC 합성에 이용되었다(Koshy, 2016; Angaru, 2021). 바닥재의 Si과 Al 성분을 확인하기 위해 실시한 XRF (X-ray fluorescence) (ZSX Primus-II, Rigaku, Japan) 분석 결과를 Table 1에 나타내었으며 Si과 Al의 비율은 각각 51.6%, 29.3%인 것으로 확인되었다.
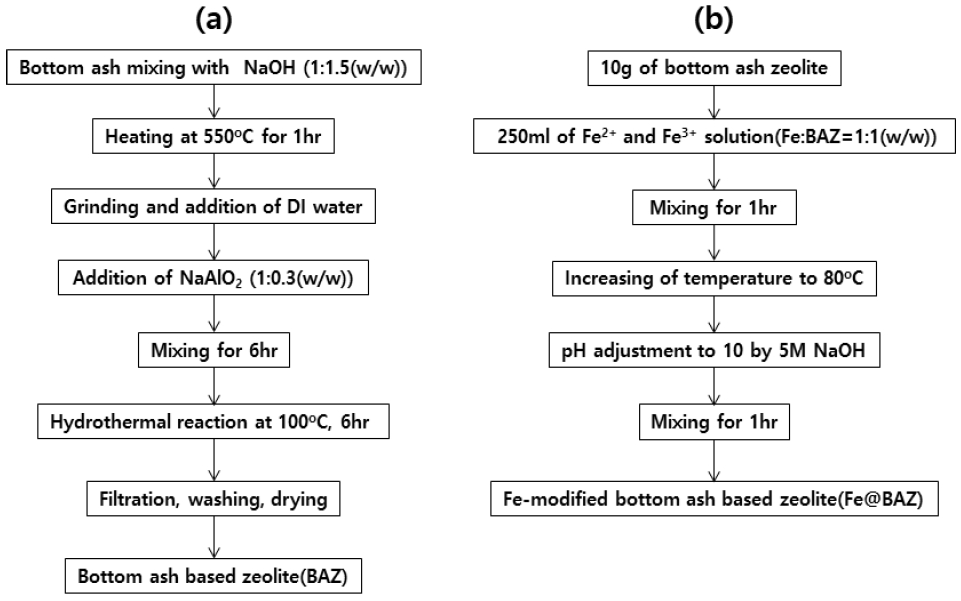
바닥재 기반 제올라이트의 합성과 철 담지를 위한 개질 방법을 Fig. 1에 나타내었다. 바닥재 기반 제올라이트 합성에는 Fusion method를 사용하였으며 이전 연구 결과를 참고하여 합성되는 제올라이트의 형태가 Na-A 제올라이트가 되도록 NaAlO2를 추가로 주입하였다(Angaru, 2021). 합성된 바닥재 기반 제올라이트 표면에 철을 담지하기 위해 Fe2+ 및 Fe3+ 용액을 사용하였으며 제올라이트와 용액 중 철의 무게 비율이 1:1이 되도록 농도를 조절하였다.
제조된 소재의 표면 결정성을 확인하기 위해 XRD 분석 (X-ray Diffractometer) (D8 Discover, Bruker, Billerica, MA, USA)을 사용하였으며 비표면적을 측정하기 위해 비표면적 및 기공분석 장치 (ASAP 2420, Micromeritics, Norcross, GA, USA)를 사용하였다.
2.2. 등온흡착실험
바닥재와 BAZ, Fe@BAZ의 비소 및 중금속에 대한 반응성을 비교 평가하기 위해 수중 As(III)와 As(V), Pb(II)를 대상으로 회분식 등온흡착실험을 실시하였다. As(III)와 As(V), Pb(II)의 농도를 각각 5~200 mg/L가 되도록 조절한 후 pH를 4로 조정하였다. 250 mL 삼각플라스크에 인공오염수 100 mL와 제조된 소재를 각각 0.01 g (Pb(II)) 또는 0.05 g (As(III), As(V))를 넣은 후 300분 동안 교반하였다. 이후 0.45 μm syringe filter를 이용하여 고액분리한 후 ICP-OES (Abio 200, Perkinelmer, MA, USA)를 통해 농도를 분석하였다. 오염물질에 대한 제거량 qe (mg/g)은 다음 식 (1)에 의해 계산 되었다.
| (1) |
여기서 여기서, C0 (mg/g)와 Ce (mg/L)는 각각 오염물질의 초기농도와 흡착 후 평형 상태의 농도를 나타내며, V는 오염수의 부피(L), W는 흡착제의 양(g)을 나타낸다. 실험을 통해 얻어진 결과와 Langmuir와 Freundlich isotherm model을 이용하여 최대흡착용량과 흡착메커니즘을 확인하고자 하였다. 식 (2)는 Langmuir isotherm model 식이며 qmax (mg/g)는 단위 질량당 최대흡착량을 의미하며 KL (L/mg)는 Langmuir 상수이다.
| (2) |
식 (3)은 Freundlich isotherm model이며 KF ([(mg/g)/(L/mg)1/n])와 n 은 각각 흡착 능력과 관련된 Freundlich 상수와 흡착 강도와 관련된 상수이며 대체로 값이 클수록 흡착효율이 높은 것으로 알려져 있다.
| (3) |
2.3. 배양실험 및 용출시험
Fe@BAZ의 비소 및 중금속 오염 퇴적물의 안정화 성능을 확인하기 위해 토양양배양실험을 실시하였다. 본 실험에서는 반월시화산업단지를 통과하는 하천인 신길천(위도 37.305277, 경도 126.748147)에서 채취하였으며 퇴적물의 비소 및 중금속의 농도와 이화학적 특성은 환경부의 토양오염공정시험기준(MOE, 2022)과 농촌진흥청의 토양화학분석법(NAAS, 2010)을 사용하였다. 오염된 퇴적물은 향후 준설되어 토양에 매립될 가능성이 있기 때문에 토양환경보전법 시행규칙의 1지역 기준치를 적용하여 검토하였다. Table 2의 퇴적물 분석 결과에 따르면 비소는 1지역 우려기준을 상회하는 것으로 나타났으며 중금속은 Cu, Pb, Zn이 1지역 대책기준을 크게 초과하는 것으로 나타났다.
안정화 성능 확인을 위한 배양실험 방법은 다음과 같다. 풍건된 퇴적물 300 g에 Fe@BAZ를 퇴적물 무게 대비 각각 2%, 5%, 7%를 적용하고 균일하게 혼합하였다. 이후 퇴적물의 함수율이 20%가 되도록 증류수를 주입하고 다시 혼합한 후 광구병에 담았다. 광구병은 밀봉하고 암조건에서 보관하였고 안정화제의 효과를 확인하기 위해 12주 동안 4주 간격으로 시료를 채취(3회)하여 용출시험에 사용하였다. 본 연구에 사용된 용출시험은 TCLP (Toxicity Characteristics Leaching Procedure) (USEPA, 1993)와 1 M NH4NO3 시험(KS ISO 19730) (KATS, 2009)이며 각각 퇴적물 중 오염물질의 이동성 및 독성과 생물유효도(Bioavailability)를 확인할 수 있는 시험방법이다. 각 용출시험의 목적 및 방법을 Table 3에 나타내었다.
3. 결과 및 고찰
3.1. Fe@BAZ 제조 결과
바닥재와 BAZ 및 Fe@BAZ의 결정성을 확인하기 위한 XRD 분석을 실시한 후 얻어진 피크 패턴을 JCPDS (Joint Committee on Powder Diffraction Standard)과 비교 하였으며 그 결과를 Fig. 2에 나타내었다. 제올라이트의 재료인 바닥재의 피크는 2θ degree 16.4, 20.8, 26.2, 26.6, 33.2, 35.2, 40.8, 50.1에서 나타났으며 이는 quartz (JCPDS No. 33-1161)와 mullite (JCPDS No. 75-8135)의 결정 구조에 기인하는 것으로 판단된다(Boycheva, 2023). Fusion method에 의해 제조된 BAZ는 2θ degree 7.2, 10.1, 12.4, 16.1, 21.6, 24.0, 27.1, 30.0, 34.11에서 피크가 관찰되었는데 이는 Na-A 제올라이트(JCPDS No. 38-0241) 결정이 형성된 것을 의미하며 기존의 관련 연구 결과들과 일치하는 것이다(Robson, 1998; Ejhieh, 2014). 또한 바닥재에서 강하게 나타난 quartz와 관련된 피크는 감소되었으며 mullite와 관련된 피크는 나타나지 않은 것으로 확인되었다. 이러한 현상은 Fusion method 방법 중 강한 알칼리 환경에서 활성화된 Si와 Al이 열과 압력에 의해 Na-A 제올라이트로 결정화되었기 때문이다. 한편 Fe@BAZ의 경우 BAZ에서 확인된 강한 피크들이 broad한 피크로 변화되었고 약 2θ 35.2에서 약한 피크가 확인되었는데 이는 철 용액을 이용한 표면개질 과정에서 BAZ 표면에 형성된 비결정질의 Fe2O3와 Fe3O4(JCPDS No. 85-1436)에 기인한 것으로 판단된다(Machala, 2007; Sharma, 2013).
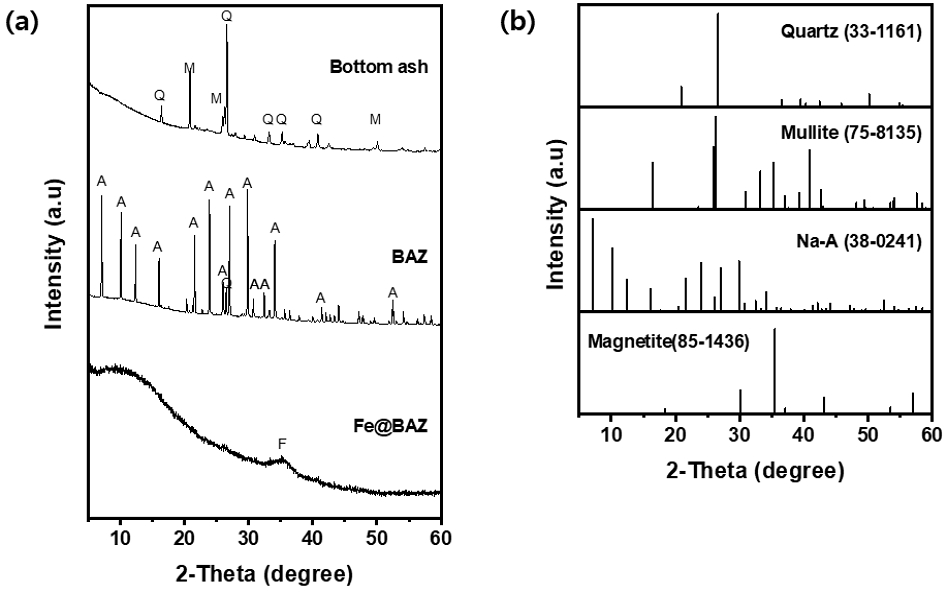
XRD patterns of (a) bottom ash, BAZ, Fe@BAZ and (b) PDF cards for quartz, mullite, Na-A, magnetite(Q=quartz, M=mullite, A=Na-X zeolite, F=Fe3O4).
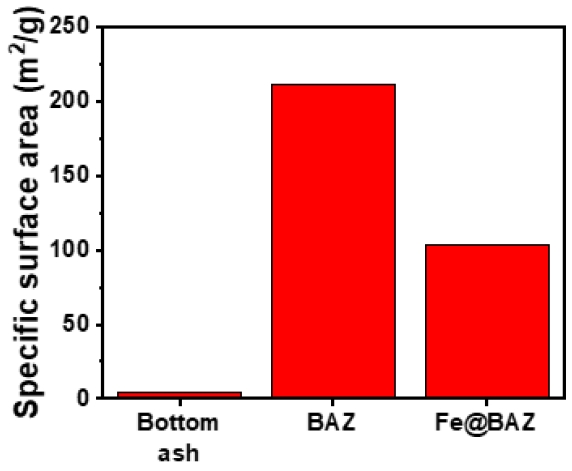
Fig. 3은 바닥재와 BAZ 및 Fe@BAZ의 비표면적을 비교한 것이다. 분석 결과에 따르면 바닥재의 BET (Brunauer, Emmett and Teller) 비표면적은 4.56 m2/g 이었으며 BAZ는 211.40 m2/g 으로 나타났으며 이는 바닥재 대비 약 46.36배 증가된 수준이다. Sowunmi et al.(2018)의 연구에 따르면 상업용 Na-A 제올라이트의 비표면적은 약 560 m2/g 이며 바닥재 대비 매우 높아진 BAZ의 비표면적은 Na-A 제올라이트의 형성에 의한 것으로 판단된다. BAZ를 이용한 표면 개질로 제조된 Fe@BAZ의 경우 비표면적이 103.27 m2/g으로 BAZ 대비 다소 감소된 것으로 확인되었다. Zhu et al.(2017)의 연구에 따르면 비결정질 Fe2O3의 비표면적은 236 m2/g으로 BAZ와 유사하며 Han et al.(2021)의 연구에 따르면 Fe3O4의 비표면적은 21.52 m2/g 으로 BAZ 대비 매우 낮은 것으로 보고되었다. 따라서 BAZ 대비 낮은 Fe@BAZ의 비표면적은 BAZ 표면에 형성된 Fe3O4에 기인한 것으로 판단된다.
3.2. 등온흡착실험 결과
Table 4는 바닥재, BAZ와 Fe@BAZ의 비소 및 중금속에 대한 반응성을 확인하기 위해 실시한 회분식 등온흡착실험에 대한 결과이다. Langmuir isotherm model를 이용한 최대 흡착용량(qmax)을 비교하였을 때 Pb(II)의 경우 바닥재와 BAZ와 Fe@BAZ의 최대 흡착용량은 각각 11.09 mg/g, 357.14 mg/g, 344.83 mg/g으로 계산되었다. BAZ의 Pb(II)에 대한 최대 흡착용량은 바닥재 대비 약 32.20배 증가된 수준을 보였으며 표면 철 개질 후 약간 감소되는 결과를 보였다. Fe@BAZ의 Pb(II)의 흡착용량은 natural zeolite (14.20 mg/g)와 Na-P1 제올라이트 (266.4 mg/g) 보다 높은 수준이며 비산재 기반 Na-X 제올라이트(420.6 mg/g) 비해 낮은 수준이다(Lee, 2000; Apiratikul, 2008; Rakhym, 2020).
As(III) 및 As(V)에 대한 흡착용량을 살펴보면 바닥재와 BAZ의 경우 흡착반응이 확인되지 않았으며 BAZ의 경우 0.44 mg/g(As(III)), 0.45 mg/g(As(V))으로 다소 낮은 수준을 보였다. 한편 Fe@BAZ의 경우 As(III) 및 As(V)에 대한 흡착용량이 각각 38.76 mg/g, 46.95 mg/g으로 BAZ 대비 매우 높은 흡착용량을 보유하는 것으로 확인되었다. 이러한 현상은 표면에 형성된 철 산화물에 의한 것으로 판단된다. 이러한 결과는 기존 연구에서 보고된 Al2O3/Fe(OH)3(As(III)=9.0 mg/g, As(V)=36.7 mg/g)대비 높은 수준이며 Cu doped Fe3O4 (As(III)=38.0 mg/g, As(V)=42.9 mg/g)와 비슷한 수준이다(Hlavay, 2005; Wang, 2015). 등온흡착실험 결과를 종합하였을 때 Fe@BAZ는 비소 및 중금속에 반응성을 가지고 있는 것으로 확인되었다. 한편 Fe@BAZ는 BAZ 대비 Pb(II)에 대한 흡착성능은 감소된 반면 As(III 및 V)에 대한 흡착 성능은 향상되었다. 이는 Fe@BAZ 제조 과정에서 BAZ와 철의 무게 비율이 1:1이 되도록 하였으며 표면에 형성된 비결정질 Fe2O3와 Fe3O4가 BAZ 대비 As(III 및 V)에 대한 반응성은 높으나 Pb(II)에 대한 반응성은 떨어지기 때문인 것으로 판단된다.
Langmuir와 Freundlich isotherm model의 상관계수(r2)를 비교하였을 때 Langmuir isotherm model이 비교적 더 높은 것으로 나타났는데 이는 Langmuir isotherm model에서 흡착 결과가 더 잘 모사되는 것을 의미하며 흡착 메커니즘이 물리적흡착 보다는 화학적 흡착에 기인하는 것을 의미한다. 이와 비슷한 연구 결과는 Angaru et al.(2021)의 연구 결과에서도 볼 수 있다. 해당 연구에서는 금속산화물에 의해 개질된 Na-A 제올라이트를 이용한 수중 음이온 및 양이온 오염물질은 제올라이트의 이온 교환과 제올라이트 표면의 산소관능기 및 철 산화물 표면에서의 착화물 형성에 의한 것으로 설명하였다.
3.3. 배양실험 및 용출시험 결과
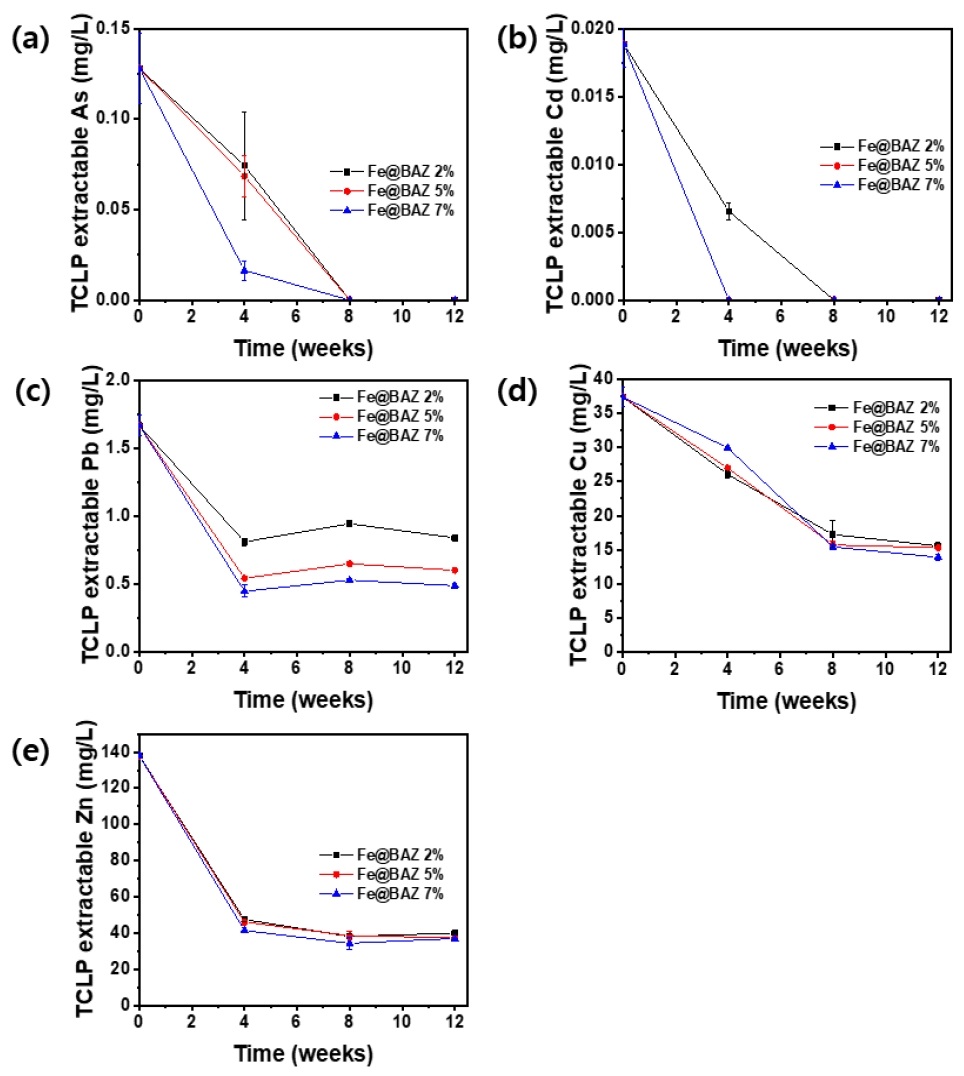
반월시화산업단지에서 채취한 실제 오염 퇴적물을 대상으로 배양실험과 용출시험을 실시하여 Fe@BAZ의 비소 및 중금속에 대한 안정화 성능을 확인하고자 하였으며 안정화 처리 기관과 적용 비율(2%, 5%, 7%)에 따른 변화를 확인하고자 하였다. Fig. 4는 퇴적물 중 오염물질의 이동성과 독성을 확인할 때 사용되는 TCLP 용출시험의 결과를 나타내고 있다. 안정화 처리 전 TCLP 용출액 중 As의 농도는 0.13, 이었으나 처리 4주 후에는 대체적으로 Fe@BAZ의 적용 비율이 증가할수록 농도가 감소되는 경향을 보였으며 처리 8주 후 부터는 모든 조건에서 검출 한계 미만 수준으로 감소되었다. Dixit et al.(2003)과 Vithanage et al.(2017)의 연구에 따르면 As(III) 및 As(V)는 산화철(Iron oxide, goethite, magnetite) 표면에서 Fe-As-O 형태의 착화물을 형성할 수 있다(식(4)~(8)).
| (4) |
| (5) |
| (6) |
| (7) |
| (8) |
Cd 또한 처리 전 농도가 0.02 mg/L이었으나 처리 8주 후에 검출 한계 미만으로 나타났다. Pb와 Zn은 처리 4주 까지 농도가 급격히 감소된 후 이후 큰 변화가 관찰되지 않았다. Pb의 경우 처리 12주 후 적용 비율 증가에 따라 안정화 효율이 큰 것으로 확인되었으며 Zn의 경우 적용 비율 변화에 따른 농도 감소의 폭이 크지 않은 것으로 확인되었다. Cu의 경우 처리 후 8주 까지는 배양 기간이 증가함에 따라 농도가 서서히 감소되었고 8주 후에는 농도가 유지되는 경향을 보였으며 적용 비율 변화에 따른 농도 변화가 크지 않았다.
As와 Cd의 농도는 안정화 처리 전 각각 0.016 mg/L, 0.014 mg/L 이었으며 안정화 처리 4주 후 부터 모든 조건에서 농도가 검출한계 미만으로 감소되었다. Pb의 경우 안정화제 적용 비율 2%, 5%의 농도 감소 효율은 비슷한 수준을 보인 반면 적용 비율 7%의 경우 비교적 높은 효율로 Pb 농도를 감소시키는 것으로 나타났다. Cu는 대체적으로 처리 후 4주 까지 농도가 급격히 감소되었으며 안정화제 적용 비율 2%에 비해 5%, 7%의 안정화 효과가 비교적 더 높은 것으로 확인되었다. Zn의 경우 처리 후 4주 까지 농도가 빠르게 감소되었으며 이후 서서히 감소되는 경향을 보였으며 안정화제 적용 비율 변화에 따른 농도 변화는 크지 않은 것으로 나타났다. 오염물질 중 미량원소를 분석하고 생물학적유효도를 알아볼 수 있는 1 M NH4NO3 용출시험에서 용출액 중 비소와 중금속의 농도가 동시에 저감되는 것이 확인되었다. 이러한 결과는 Fe@BAZ를 오염 퇴적물에 적용하였을 때 이동성 비소 및 중금속이 식물체로 전이되는 과정을 차단할 수 있는 것을 의미하며 결과적으로 오염 퇴적물 중 생물학적유효도를 저감할 수 있는 것을 의미한다.
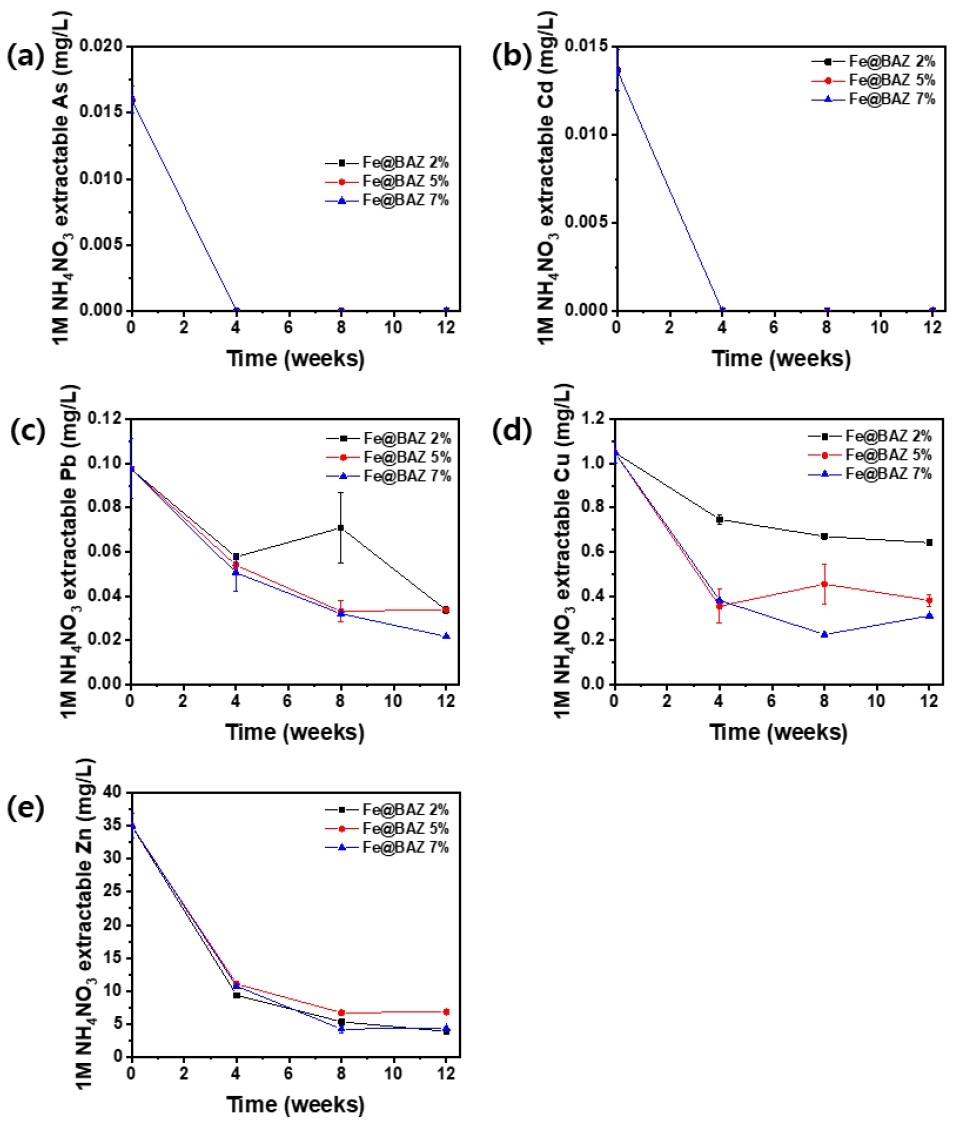
1 M NH4NO3 extractable arsenic and heavy metals concentrations; (a) As, (b) Cd, (c) Pb, (d) Cu, (e) Zn.
TCLP 및 1 M NH4NO3 용출시험 결과에 따르면 안정화제로서 Fe@BAZ는 오염 퇴적물 중 비소 및 중금속을 동시에 안정화할 수 있는 것으로 확인되었다. 상기의 특성평가와 회분식 등온흡착실험 결과를 종합하였을 때 Fe@BAZ는 Na-A 제올라이트의 양이온 교환 능력을 기반으로 중금속에 대한 높은 반응성을 가지는 것으로 확인되었다. 또한 표면 개질 이후 비소와 반응하여 착화물 형성할 수 있는 비결정질 Fe2O3 및 Fe3O4를 보유하기 때문에 비소에 대한 반응성을 보유하는 것으로 확인되었다. 이러한 특성을 가지는 Fe@BAZ는 오염 퇴적물 중 비소 및 중금속을 효과적으로 안정화 할 수 있는 것으로 판단된다. 이러한 결과를 고려할 때 Fe@BAZ는 오염 퇴적물 중 비소 및 중금속의 이동성 및 생물학적유효도를 감소시킴으로써 위해성을 저감할 수 있는 소재로 적용이 가능한 것으로 예상된다.
4. 결 론
본 연구에서는 오염 퇴적물 중 비소 및 중금속의 안정화를 통해 위해성을 저감할 수 있는 철 개질 바닥재 기반 제올라이트인 Fe@BAZ를 제조하였다. 또한 바닥재, BAZ와 Fe@BAZ의 특성과 비소 및 중금속에 대한 반응성을 확인하고자 하였으며 실제 오염 퇴적물을 이용한 배양실험을 통해 안정화제로서 Fe@BAZ의 성능을 평가하고자 하였다. 본 연구에서 얻은 결론은 다음과 같다. Fusion method를 이용하여 화력발전소에서 채취한 바닥재로부터 Na-A 형태의 제올라이트를 합성하고 이후 철 용액을 이용하여 표면 개질 하였을 때 형성되는 물질은 Fe3O4와 비결정질의 Fe2O3인 것으로 확인되었다. Fe@BAZ는 기존 소재 대비 Pb(II)와 As(III) 및 As(V)에 대한 흡착용량이 우수한 것으로 나타났는데 이는 Na-A 제올라이트의 중금속에 대한 반응성과 Fe3O4와 비결정질의 Fe2O3의 비소에 대한 반응성을 모두 보유하기 때문이다. 실제 비소 및 중금속에 의해 오염된 퇴적물을 대상으로 배양실험을 실시하여 안정화제로서 Fe@BAZ의 성능을 평가하였으며 TCLP와 1 M NH4NO3 용출시험 결과 비소 및 중금속을 동시에 안정화함으로써 위해성을 저감할 수 있는 것이 확인되었다. Fe@BAZ는 화력발전소에서 배출되는 바닥재를 고부가가치 자원으로 활용할 수 있으며 매립되는 오염 퇴적물의 위해성을 저감시킬 수 있는 다기능성 소재이기 때문에 활용 가능성이 높을 것으로 예상된다.
Acknowledgments
본 연구는 2024년도 안산녹색환경지원센터의 지원(24-07-04-60-61)과 한국환경산업기술원의 지원(RS-2023-00230451)을 받아 수행된 연구입니다.
REFERENCES
-
Apiratikul, R., Pavasant, P., 2018, Sorption of Cu2+, Cd2+, and Pb2+ using modified zeolite from coal fly ash, Chem. Eng. J., 144, 245–258.
[https://doi.org/10.1016/j.cej.2008.01.038]

-
Angaru, G. K. R., Choi, Y. L., Lingamdinne, L. P., Choi, J. S., Kim, D. S., Koduru, J. R., Chang, Y. Y., 2021, Facile synthesis of economical feasible fly ash–based zeolite–supported nano zerovalent iron and nickel bimetallic composite for the potential removal of heavy metals from industrial effluents, Chemosphere, 267, 128889.
[https://doi.org/10.1016/j.chemosphere.2020.128889]

-
Angaru, G. K. R., Choi, Y. L., Lingamdinne, L. P., Koduru, J. R., Yang, J. K., Chang, Y. Y., Karri, R. R., 2022, Portable SA/CMC entrapped bimetallic magnetic fly ash zeolite spheres for heavy metals contaminated industrial effluents treatment via batch and column studies, Scientific Reports, 12, 3430.
[https://doi.org/10.1038/s41598-022-07274-5]

-
Boycheva, S., Szegedi, A., Lazar, A., Popov, C., Popova, M., 2023, Advanced high-iron coal fly ash zeolites for low-carbon emission catalytic combustion of VOCs, Catalysis Today, 418, 114109.
[https://doi.org/10.1016/j.cattod.2023.114109]

-
Dean, C. M., Sansalone, J. J., Carledge F. K., Pardue, J. H., 2005, Influence of hydrology on rainfall-runoff metal elements speciation, J. Environ. Eng., 131, 632-642.
[https://doi.org/10.1061/(ASCE)0733-9372(2005)131:4(632)]

-
Dixit, S., Hering, J. G., 2003, Comparison of Arsenic(V) and Arsenic(III) sorption onto iron oxide minerals: implications for arsenic mobility, Environ. Sci. Technol., 37, 4182-4189.
[https://doi.org/10.1021/es030309t]

-
Ejhieh, A. N., Banan, Z., 2014, Photodegradation of dimethyldisulfide by heterogeneous catalysis using nanoCdS and nanoCdO embedded on the zeolite A synthesized from waste porcelain, Desalin. Water Treat., 52, 3328-3337.
[https://doi.org/10.1080/19443994.2013.797627]

-
Han, J. S., Am, G. S., 2021, Preparation of dual-layered core–shell Fe3O4@SiO2 nanoparticles and their properties of plasmid DNA purification, Nanomaterials, 11, 3422.
[https://doi.org/10.3390/nano11123422]

-
Hlavay, J., Polyak, K., 2005, Determination of surface properties of iron hydroxide-coated alumina adsorbent prepared for removal of arsenic from drinking water, J. Colloid Interface Sci., 284, 71-77.
[https://doi.org/10.1016/j.jcis.2004.10.032]

-
Jeong, H. R., Lee, J. H., Choi, J. Y., Kim, K. T., Kim, E. S., Ra, K. T., 2019, Assessment of contamination and sources identification of heavy metals in stream water and sediments around industrial complex, Korean J. Ecology and Environment, 52, 179-191.
[https://doi.org/10.11614/KSL.2019.52.3.179]

- Jung, J. Y., 2014, Characteristics of waterborne sediments and management measures of dredged sediments, Master Dissertation, Kwangwoon University, Seoul, Korea.
- KEI, 2014, Minimizing environmental impact accordance with the thermal power plant ash management, Final report 2014-02-01, KEI, Korea.
-
Koshy, N., Singh, D. N., 2016, Fly ash zeolites for water treatment applications, Journal of Environmental Chemical Engineering, 4, 1460-1472.
[https://doi.org/10.1016/j.jece.2016.02.002]

-
Lee, M. G., Yi, G., Ahn, B. J., Roddick, F., 2000, Conversion of coal fly ash into zeolite and heavy metal removal characteristics of the products, Korean J. Chem. Eng., 17, 325–331.
[https://doi.org/10.1007/BF02699048]

-
Machala, L., Zboril, R., Gedanken, A., 2007, Amorphous Iron(III) oxide-A Review, J. Phys. Chem. B, 111, 4003-4018.
[https://doi.org/10.1021/jp064992s]

- MOE, 2022, Korean standard test methods for soils, Korean Ministry of Environment.
- NAAS, 2010, Methods of soil chemical analysis, Rural Development Administration, Korea.
-
Rakhym, A. B., Seilkhanova, G. A., Kurmanbayeva, T. S., 2020, Adsorption of lead(II) ions from water solutions with natural zeolite and chamotte clay, Materials Today, 31, 482-485.
[https://doi.org/10.1016/j.matpr.2020.05.672]

- Robson, H., 1998, Verified synthesis of zeolitic materials, Micropor. Mesopour. Mater., 22, 551–666.
-
Sharma, G., Jeevanandam, P., 2013, Synthesis of self-assembled prismatic iron oxide nanoparticles by a novel thermal decomposition route, RSC Advances, 3, 189-200.
[https://doi.org/10.1039/C2RA22004K]

-
Sowunmi, A. R., Folayan, C. O., Anafi, F. O., Ajayi, O. A., Omisanya, N. O., Obada, D.O., Dodoo-Arhin, D., 2018, Dataset on the comparison of synthesized and commercial zeolites for potential solar adsorption refrigerating system, Data in Brief, 20, 90-95.
[https://doi.org/10.1016/j.dib.2018.07.040]

-
Sun, Y., Zhang, D., Li, F., Tao, H., Li, M., Mao, L., Gu, Z., Liang, Z., Shi, H., 2020, The rainfall effect onto solidification and stabilization of heavymetal-polluted sediments, Royal Society Open Science, 7, 192234.
[https://doi.org/10.1098/rsos.192234]

- USEPA, 1993, Selecting remediation techniques For contaminated sediment, EPA-823-B93-001.
-
Vithange, M. M., Hearth, I., Joseph, S., Budndschuh, J., Bolan, N., Ok, Y. S., Kirkham, M. B., Rinklebe, J.. 2016, Interaction of arsenic with biochar in soil and water: A Critical review, Carbon, 113, 219-230.
[https://doi.org/10.1016/j.carbon.2016.11.032]

-
Wang, T., Yang, W., Song, T., Li, C., Zhang, L., Wang, H., Chai, L., 2015, Cu doped Fe3O4 magnetic adsorbent for arsenic: Synthesis, property, and sorption application, RSC Advances, 5, 50011-50018.
[https://doi.org/10.1039/C5RA03951G]

- Yang, Y. M., Chae, M. H., Lee, D. H., Kil, G. B., Kim, D. H., Cho, Y. H., Cheon, S. O., 2019, Spatial distribution and pollution assessment of metals in the sediments of a gap stream Korea, J. of the Korean Society for Environmental Analysis, 22, 50-60.
-
Zhu, X., Jinang, X., Chen, X., Liu, X., Xiao, L., Cao, Y., 2017, Fe2O3 amorphous nanoparticles/graphene composite as high-performance anode materials for lithium-ion batteries, J. Alloys Compd., 77, 15-21.
[https://doi.org/10.1016/j.jallcom.2017.03.235]

Department of Environmental Engineering, Kwangwoon Universityryans85@naver.com
Department of Environmental Engineering, Kwangwoon Universityshinbom@hanmail.net
Department of Environmental Engineering, Kwangwoon Universityjangunbu@hanmail.net
Department of Environmental Engineering, Kwangwoon Universityjungjy38@naver.com
Department of Environmental Engineering, Kwangwoon Universityluckypax@naver.com
Department of Environmental Engineering, Kwangwoon Universitymsy@dohwa.co.kr
Department of Environmental Engineering, Kwangwoon Universityyychang@kw.ac.kr