오존 용존율 증대를 통한 전기-페록손 공정의 성능 향상
Ⓒ The Korean Environmental Sciences Society. All rights reserved.
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Traditional wastewater treatments, such as biological treatments, were not designed to treat persistent drugs in wastewater such as acetaminophen. Therefore, these treatments are unsuitable for treating wastewater containing pharmaceuticals. Currently, pharmaceuticals are treated and do not completely decompose, entering aquatic environments. Advanced oxidation processes (AOPs) are among most efficient modern technologies for treating wastewater contaminated with nonbiodegradable organic pollutants. The electro-peroxone process is currently receiving attention as an ozone-based AOP because this process increases the decomposition of difficult-to-decompose pollutants and suppresses the production of toxic byproducts. This study developed a method to increase the ozone dissolution rate and thus the efficiency of the electro-peroxone process. This study also evaluated the possibility of increasing of the ozone dissolution rate and improving the performance of the electro-peroxone process.
Keywords:
Acetaminophen degradation, Electro-peroxon process, Ozone dissolution, TOC removal1. 서 론
최근 의약품 및 개인 위생용품의 사용량이 증가하고 있고, 이들 물질이 새로운 난분해성 오염물질의 한 부분을 차지하고 있다(Reyes et al., 2021). 이들 의약품 중 아세트아미노펜은 감기나 독감, 해열진통제로 널리 사용되는 의약물로 처방전 없이 쉽게 구할 수 있고, 중독 가능성이 높은 물질로, 코로나19 등으로 생산 및 사용량이 증가하여, 수계에서 검출되는 농도가 증가하고 있는 것으로 알려져 있다(Pashaei et al., 2022). 아세트아미노펜과 같은 화합물은 섭취 후 사람이나 동물의 불완전한 대사로 인해 수계에 유입되거나 미사용 의약품이 올바르게 폐기되지 않고 수계에 유입되기도 한다(Byeon et al., 2024).
현재 하·폐수 처리에 적용되고 있는 생물학적 처리와 같은 전통적인 처리 기술은 아세트아미노펜과 같은 난분해성 의약품을 처리하도록 설계되지 않아 의약물질 처리에 적합하지 않고 완전히 분해되지 않고 처리되어 수생환경에 유입되고 있는 것으로 알려져 있다(Reyes et al., 2021). 또한 아세트아미노펜의 분해 과정 중 생성된 중간 생성물은 기존 의약물질보다 더 강한 독성을 유발할 수 있어 수중에 잔류할 경우 수중 생태계에 잠재적인 악영향을 가져올 수 있다(Kim et al., 2009).
의약물질의 효율적인 분해를 위해 연구된 처리 기술 중에서 고급산화 공정(AOPs, Advanced oxidation processes)은 유기 오염물질로 오염된 폐수를 처리하는 가장 효율적인 현대 기술 중 하나이다. 고급산화 공정은 수산기 라디칼(·OH)과 같은 활성 산소종(ROS, Reactive oxygen species)을 현장에서 생성하여 처리에 이용할 수 있으며, 난분해성 유기 오염물질을 비선택적으로 공격할 수 있는 강력한 산화제를 생성하여 광범위한 유기 화합물을 빠르게 산화하여 무기화까지 가능한 것으로 알려져 있다(Felisardo et al., 2024; Rashidi et al., 2024).
오존 기반의 고급산화 공정은 펜톤 산화와 비교하여 슬러지가 없다는 장점이 있어 산업적으로 매력적인 공정으로, 현장 적용시 운영 비용이 현저하게 낮은 것으로 알려져 있다. 오존은 촉매, 자외선 램프, H2O2 등과의 반응에 의하여 ·OH을 생성할 수 있다. 이러한 방법 중 오존과 H2O2의 반응에 의하여 ·OH을 생성하는 공정을 페록손(Peroxone) 공정이라고 하며, 페록손 공정은 현재 난분해성 오염물질의 분해를 향상시키고 독성 부산물 생성을 억제할 수 있어 주목을 받고 있는 공정이다(Zhang et al., 2024).
그러나, H2O2는 다른 물질과의 반응성이 높고, 특히 실험실이 아닌 현장에서 대량의 H2O2를 저장하고 운반하는 것은 안전하지 않고 위험성이 높다. 따라서 이를 해결하기 위하여 최근 오존 발생기를 사용하여 생성하고, H2O2는 전극에 의한 전기분해 반응을 통하여 산소의 음극 현장 환원을 통해 생성하는 전기-페록손(Electro-peroxone) 공정이 연구되고 있다(Shokri and Nasernejad, 2024). 페록손 반응이나 전기-페록손 반응에서 중요한 역할을 하는 오존은 물에 대한 용해도가 0℃에서 1부피의 물에 대해 0.494 vol%로 낮기 때문에 오존의 용해도 증가는 오존과 전기분해 반응에서 발생하는 과산화수소를 이용하여 ·OH을 발생시키는 전기-페록손 성능에 영향을 주는 중요한 요소이다(Water Encyclopedia, 2016).
본 연구는 전기-페록손 공정의 효율을 증가시키기 위하여 오존 용존율을 상승시키는 방법에 대한 연구를 진행하여 오존의 용존율 향상에 대한 가능성과 전기-페록손 공정의 성능을 평가하고자 하였다.
2. 재료 및 방법
2.1. 실험장치 및 방법
1) 실험장치
실험은 2단계로 이루어져 있으며, 1단계는 전기-페록손 공정의 성능 향상을 위해 오존의 용존율을 높이기 위한 새로운 오존 공급방법에 관한 내용이다. 2단계는 기존 오존 단일공정과 새로운 오존 공급시스템을 채택한 전기-페록손 공정의 성능 비교 실험이다.
① 오존 공급방법의 변경
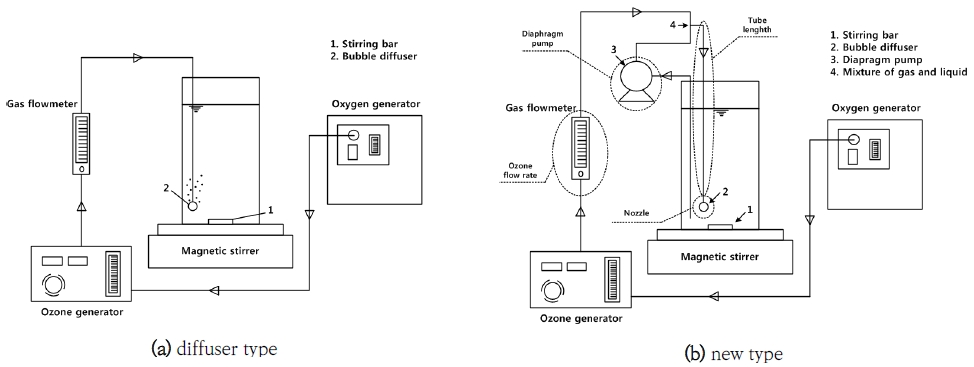
전기-페록손 공정에서 일반적인 오존 공급시스템은 Fig. 1(a)에서 보는 바와 같이 오존 발생장치에서 발생한 오존 가스를 산기관(Diffuser)을 이용하여 반응기 내부의 수중에 바로 배출하여 반응에 이용한다.
오존의 용존율을 높이기 위하여 오존 가스가 배출되는 시스템을 기존의 산기관 방식에서 5종류[배출 구경이 다양한 액체 분사용 원형 분사노즐(1.6, 2.3 3.2 mm nozzle), 이류체(二流體) 분사노즐(Air-automizing nozzle), 배출구가 3개인 3구 노즐(3-rong nozzle)]의 노즐을 이용하는 노즐식으로 변경하였다(Kim and Park, 2018). Fig. 1(b)에 나타낸 바와 같이 이류체 노즐을 제외한 4종류의 노즐방식(1.6, 2.3 3.2 mm nozzl 및 3구 노즐)은 오존 발생장치에서 발생하는 오존 가스를 반응기로 바로 유입시키지 않고 액체순환 펌프를 이용하여 반응기 내의 물을 T자형 피팅으로 각각 유입시킨 후 T자형 피팅에서 기-액 혼합물이 1차 혼합되면서 혼합관을 통하여 노즐 내부에서 다시 혼합된 후 노즐을 통하여 반응기로 배출하였다. 이류체 노즐은 T자형 피팅을 거치지 않고 노즐 좌우의 유입구에 오존 가스와 순환수가 각각 유입된 후 노즐에서 1차 혼합되어 수중으로 배출되는 형태이다.
② 액체 순환유량의 영향
액체 순환유량 변경은 오존 발생장치의 전력이 120 W인 조건에서 오존 유량은 0.5 L/min, 3구 노즐을 이용하여 액체 순환펌프에 인가되는 전압(30 ~ 70 V)을 조절하여 반응기에서 노즐로 공급하여 순환시키는 반응액의 유량을 642 mL/min, 1,066 mL/min, 1,490 mL/min, 1,914 mL/min, 2,338 mL/min로 변경하면서 실험하였다.
③ 오존 가스유량의 영향
오존 가스유량은 3구 노즐을 이용하고 액체 순환펌프 유량을 1,914 mL/min로 고정한 조건에서 오존 발생장치에서 반응기로 들어오는 공기 유량을 0.5 ~ 3.0 L/min로 변경하여 생성되는 오존 가스의 유량을 변경하였다.
④ 혼합관 길이의 영향
오존 가스와 반응기 내의 물이 T자형 피팅에서 혼합된 후 노즐을 거쳐 반응기로 들어갈 때 T자형 피팅과 노즐과의 거리인 혼합관의 길이가 오존의 용존에 영향을 준다고 판단하여 혼합관 길이를 변경하여 오존 용존율 변화를 평가하였다. 오존 발생장치에서 배출되는 오존 가스와 액체 순환펌프에 의해 순환하는 액체가 만나는 지점인 T피팅(Fig. 1(b)의 4번 지점)부터 3구 노즐(Fig. 1(b)의 2번 지점)까지의 혼합관 길이를 0.5 ~ 3 m로 50 cm씩 변화시켜 실험하였다. 이때 3구 노즐을 이용하고 액체 펌프유량은 1,914 mL/min, 오존 가스 유량은 1.5 L/min으로 고정하여 실험하였다.
2) 실험 방법
반응기는 부피가 1.5 L(직경 8.5 cm, 높이 30 cm) 비이커를 사용하였고, 반응 부피는 1 L이었다. 아세트아미노펜 분해반응 동안 마그네틱 교반기로 200 rpm으로 교반하였으며 초기 아세트아미노펜의 농도는 10 mg/L이었다. 오존은 산소 발생장치(2.IND-7.5LC, OXUS, Korea)를 사용해서 산소(O2 > 90%)를 생성시킨 후 오존 발생장치(LAB 2, Ozone Tech, Korea)에 공급하여 오존(O3) 가스를 발생시켰고, 오존 농도는 오존 발생장치의 전력을 변경하여 조절하였다. 오존 발생장치에서 반응기로 들어오는 오존 유량은 산기관인 경우 반응 초기에 0.5 L/min로 고정하였고, 노즐을 이용하는 시스템에서는 0.5 ∼ 3.0 L/min까지 변화시켜 실험하였다(Kim, 2018). 반응기 내의 액체를 노즐로 공급하는 액체 순환펌프(Diaphragm pump 2088-564-144, SHURFIO)는 전압을 30 V(642 mL/min) ∼ 70 V (2,338 mL/min)로 조절하여 액체 유량을 변경하여 실험하였다.
오존 공급방법 변경에서 얻은 조건에 전기분해 공정을 도입한 전기-페록손 공정 실험을 실시하였다. 전기분해에 사용한 전극은 양극과 음극 모두 Ti-Ir-Ru 3성분인 산화물 전극(DSA, Dimensionally stable anode)을 사용하였고 전극의 면적은 25 cm2이었다. 전기분해를 위한 전해질로 0.05 M Na2SO4를 투입하였다. Fig. 1(b)의 새로운 유형의 오존 공급장치를 이용한 반응기에 전극을 투입하여 실험을 실시하였다.
2.2. 분석 및 측정 방법
아세트아미노펜(Acetaminophen, Sigma-Aldrich)을 비롯한 실험에 사용한 약품과 시약은 모두 1등급 시약을 사용하였고, 모든 용액은 Mill-Q system (NANO pure Diamond, Barnstead, USA)으로 처리한 초순수를 사용하였다.
아세트아미노펜 용액은 10,000 ppm인 원액을 제조한 후, 10 ppm으로 희석하여 사용하였다. 용존 오존농도는 인디고 실험법으로 측정하였다(Bader et al., 1981). 아세트아미노펜 농도는 HPLC (LC-10AD, Shimadzu, Japan)를 사용하여 측정하였으며, 분석 칼럼은 LiChroCART 250-4 LiChrospher 100 RP-18 column (5 μm, 250 mm × 4 mm, Merck, Germany)을 사용하였다. 오븐 온도는 40℃, 검출기 파장은 248 nm, 이동상은 30%의 메탄올, 70%의 초순수를 사용했으며 유입 유량은 0.5 mL/min인 조건으로 분석을 실시하였다(Zhang et al., 2017).
또한, 아세트아미노펜의 무기화와 중간 생성물의 분해를 비교하기 위해서 TOC 분석기(TOC-5000A, Shimadzu, Japan)를 사용하여 Total organic carbon (TOC) 농도를 측정하였다. 총 잔류 산화제(TRO, Total residual oxidants)는 DPD total Chlorine reagent (Hach, Loveland, USA) 시약을 시료에 투입하여 발생하는 발색 정도를 Hach 수질분석기(DR 2800, Hach, Loveland, USA)를 사용하여 측정하였다(Park et al., 2010). 전력소비량은 전력량측정기(SJPM-C16N, Seojun, Korea)에 기기를 연결하여 실제 전력소비량을 측정하였다.
3. 결과 및 고찰
3.1. 오존 공급방법의 변경이 아세트아미노펜 분해에 미치는 영향
Li et al.(2014)은 전기-페록손 공정에서 전기분해 공정으로 생성된 과산화수소의 농도와 충분히 반응할 오존이 발생하면 이들의 반응에 의해 생성되는 ·OH 농도도 직선적으로 증가하지만, 오존의 용해도가 낮기 때문에 결국 ·OH 생성률은 기상에서 액상으로의 오존 물질전달 때문에 제한된다고 보고하였다. 따라서 본 실험은 오존의 용존율을 높이는 것이 전기-페록손 공정의 주요 공정인 오존 공정의 성능을 향상할 수 있다고 판단하여 용존율이 낮은 오존의 용해율을 증가시키기 위하여 오존 발생장치에서 발생하는 오존 가스를 산기관을 이용하여 오존을 배출하는 기존 방법과 오존을 수중에 바로 유입시키지 않고 액체 순환펌프를 통하여 반응기 내의 반응액을 순환시킨 순환수와 노즐을 통하여 혼합시킨 후 수중에 분사하는 방법으로 오존의 용존율을 높이는 방법의 타당성을 아세트아미노펜 분해를 통하여 평가하였다. 오존 발생장치에서 발생하는 오존 가스유량은 0.5 L/min, 순환수 유량은 1,914 mL/min, T자형 피팅에서 오존 가스-반응액 혼합 유체 배출장치인 노즐까지의 혼합관 길이는 50 cm이었다.
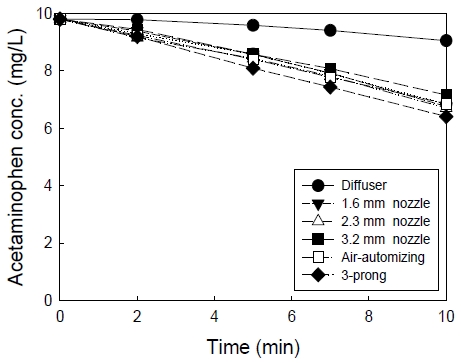
Fig. 2에 세라믹 산기관과 5 종류의 노즐을 이용하여 오존 가스를 분사하였을 때의 아세트아미노펜 분해를 나타내었다. 세라믹 산기관을 이용하여 오존 가스를 수중에 직접 분사하는 경우, 아세트아미노펜 농도는 직선적으로 감소하여 초기 10 mg/L에서 10분 경과 후 9.05 mg/L로 9.5%의 아세트아미노펜이 분해되었다.
노즐을 이용하는 경우는 아세트아미노펜 분해가 모두 산기관보다 증가하는 것으로 나타났다. 아세트아미노펜 분해 정도는 3.2 mm 노즐 < 2.3 mm 노즐 <≒ 1.6 mm 노즐 <≒ 이류체 노즐 < 3구 노즐로 나타났다. 노즐식의 경우 노즐 직경이 3.2 mm 분사노즐은 반응 10분 후 7.15 mg/L(제거율 28.5%), 아세트아미노펜 분해가 가장 높았던 3구 노즐의 경우 6.41 mg/L(제거율 35.9%)로 나타나 노즐로 오존 가스와 반응기 내의 물을 혼합하는 방식은 산기관보다 3 ~ 3.8배 높은 것으로 나타나 오존 가스를 수중에 바로 산기시키는 방식보다 우수한 것으로 판단되었고, 배출구가 1개인 노즐(원형 분사노즐, 이류체 노즐 )보다 배출구가 3개인 3구 노즐의 성능이 가장 우수한 것으로 나타났다. 본 실험과 유사한 노즐을 이용하여 수중의 용존산소 증가에 대해 고찰한 결과 노즐을 이용하는 것이 산기관을 이용하는 방식보다 수중 용존산소 농도가 높았다는 Kim and Park(2018)의 결과와 비슷한 결과를 나타내었다. 산기관을 비롯한 실험에 사용한 5종류의 오존 가스-반응액 혼합 유체 분사장치 중에서 잔류 아세트아미노펜 농도가 가장 낮았던 3구 노즐을 이용하여 다음 실험을 진행하였다.
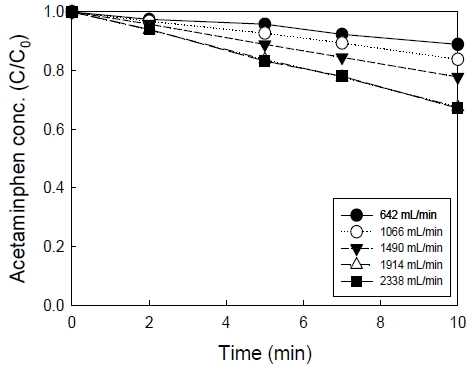
3구 노즐을 사용하고 오존 발생장치 전력 120 W, 혼합관 길이 50 cm, 오존 가스유량 0.5 L/min인 조건에서 순환펌프의 전압을 30~70 V로 변화시켜 액체 순환유량을 642(30 V), 1,066, 1,490, 1,914 및 2,338 mL/min(70 V)로 변화시켜 액체 순환유량이 아세트아미노펜 분해에 미치는 영향을 고찰하여 Fig. 3에 나타내었다.
액체 순환유량이 가장 낮은 642 mL/min에서 잔류 아세트아미노펜 농도는 10분에 8.89 mg/L로 나타나 11.1%의 제거율을 나타내었다. 액체 순환유량이 증가하면서 잔류 아세트아미노펜 농도가 감소하여 1,914 mg/L에서 잔류 아세트아미노펜 농도는 6.72 mg/L로 32.8%의 제거효율을 나타내었고, 액체 순환유량이 2,338 mL/min으로 증가하였을 때 잔류 아세트아미노펜 농도는 6.71 mg/L, 제거효율은 32.9%로 나타났다. 1,914 mL/min 이상의 액체 순환유량에서 아세트아미노펜 제거율이 상승되지 않아 최적 액체 순환유량은 1,914 mL/min인 것으로 나타났다.
액체 순환유량의 증가는 혼합관에서의 오존 가스와 반응액과의 접촉을 증가시켜 오존의 용존이 증가되는 역할을 하는 것으로 판단되었다. 오존 가스와 순환되는 액체가 혼합되는 혼합관을 육안으로 관찰한 결과 최적 순환유량 이상에서는 빠르게 순환하는 액체가 오존 가스의 유입을 방해하여 골고루 섞이지 못하고 유입되는 오존 가스의 유량이 변동하는 현상이 발생하였으며, 이 현상 때문에 혼합이 더 잘되지 않아 더 이상의 아세트아미노펜 분해가 일어나지 않는다고 판단되었고, 향후 실험은 1,914 mL/min의 액체 순환유량에서 실험을 진행하였다.
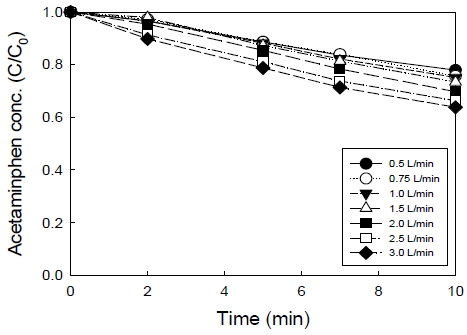
3구 노즐, 오존 발생장치 전력 120 W, 액체 순환유량 1,914 mL/min, 혼합관 거리 50 cm인 조건에서, 오존 발생기로 공급되는 산소의 유량을 변경하여 오존 발생기에서 배출되는 오존 가스의 유량을 0.5 L/min에서 3.0 L/min으로 변경하여 오존 가스유량이 아세트아미노펜 분해에 미치는 영향을 고찰하여 Fig. 4에 나타내었다.
오존 가스유량이 0.5 L/min에서 10분 경과시 잔류 아세트아미노펜 농도는 7.79 mg/L로 22.1%의 제거율을 나타내었다. 오존 가스유량이 0.5 L/min에서 3.0 L/min으로 증가하면서 잔류 아세트아미노펜 농도가 직선적으로 감소하여 6.38 mg/L로 감소하였으며, 36.2%의 제거율을 나타내었고, 제거율 차이는 약 1.6배에 달하는 것으로 나타났다. 오존 발생장치에 인가되는 전력이 같고 오존 발생장치로 공급되는 공기의 유량만 변한 조건에서 오존이 생성되므로 0.5 L/min의 오존 가스유량은 고농도의 오존 가스가 배출되고, 3.0 L/min에서는 저농도의 오존 가스가 배출된다고 판단된다. 오존 가스유량이 큰 경우 반응액과 접촉할 수 있는 오존 가스의 양이 많으므로 오존의 용해에 유리하다고 판단되었다. 그러나 본 실험에서의 향후 운전 가스유량은 3.0 L/min이 아니라 1.5 L/min으로 결정하였다. 이는 일부 오존 가스 유량에서 반응기 운전시 이상이 발생되어 육안으로 관찰한 결과 2.0 L/min의 오존 가스 유량에서는 오존 발생기로 산소를 공급하는 산소 발생장치가 정지하는 경우가 발생하였고 가스유량이 증가하면서 정지하는 경우가 다수 발생하였다. 이는 오존 가스-반응액 혼합유체가 내경이 6 mm인 관을 통해 3구 노즐로 유입되는데, 오존 가스의 유량이 증가하면 순환하는 액체와 같이 T자형 피팅으로 유입되는 관 내부에 압력이 걸리면서 오존 발생장치에 역으로 압력이 걸려 운전이 정지하는 것으로 판단되었다. 또한 가스유량이 많은 경우는 물과 혼합되지 못하고 과량의 가스가 노즐로 배출되어 배출되는 기포의 크기가 커지는 현상도 관찰되었다. 3.1.2절에서 관찰한 바와 같이 기체나 액체의 한 쪽의 유입 비율이 높은 경우 다른 쪽의 유입과 기-액 혼합에 영향을 주므로 액체 순환유량과 가스유량이 적절한 비율로 혼합되어야 기-액 혼합이 증가한다고 판단되었다. 관내 흐름에 있어 공동화 현상(cavitation)이 발생하지 않는 오존가스 유량/액체 유량(L gas/L liquid) 비는 약 0.8로 나타났고, 향후 운전은 장치의 운전에 영향을 받지 않는 유량인 1.5 L/min을 오존 가스유량으로 결정한 후 실험하였다.
오존 발생장치에서 발생한 오존 가스와 액체 순환펌프에서 순환하는 반응기 내의 순환수가 T자형 피팅에서 접촉한 후 혼합된 유체가 혼합관을 따라 3구 노즐을 통해 반응기로 배출된다. 따라서 오존 가스와 반응기 내 순환수가 만나는 혼합관 길이가 오존 가스의 용해에 영향을 미친다고 판단하여 T자형 피팅에서 3구 노즐까지의 혼합관 길이가 아세트아미노펜의 분해에 미치는 영향을 고찰하였다.
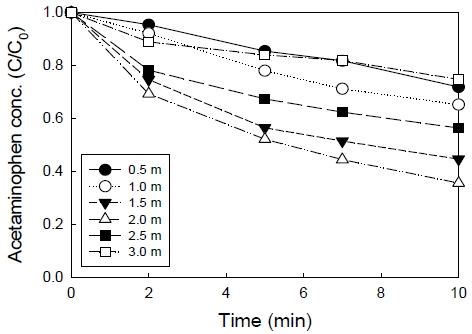
오존 발생장치 전력 120 W, 액체 순환유량 1,914 mL/min, 오존 가스유량 1.5 L/min인 조건에서 혼합관의 길이를 0.5 ~ 3.0 m까지 변화시켜 혼합관의 길이가 아세트아미노펜 분해에 미치는 영향을 고찰하여 Fig. 5에 나타내었다.
Fig. 5에서 보듯이, 혼합관의 길이가 0.5 m인 경우 반응 10분 후 잔류 아세트아미노펜 농도는 7.18 mg/L(제거율, 28.2%)이었으며, 혼합관 길이가 2.0 m에 이르기까지 잔류 아세트아미노펜 농도가 감소하였다. 반응 10분 후 관 길이가 2.0 m에서 잔류 아세트아미노펜 농도는 3.55 mg/L(제거율, 64.5%)로 0.5 m보다 제거율이 2.28배 증가하여 관 길이가 길 경우 관 내에서 오존 가스와 반응액과의 접촉과 혼합이 증가하여 아세트아미노펜 분해율이 높아진다고 판단되었다.
그러나 관 길이가 2.5 m로 증가하면서 10분 후 잔류 아세트아미노펜 농도가 5.63 mg/L, 3.0 m에서는 7.47 mg/L로 증가하여 2.5 m 이상의 관 길이에서는 길이가 증가할수록 아세트아미노펜의 분해가 방해를 받는 것으로 나타났다. 이 현상을 파악하기 위하여 육안으로 혼합관과 오존 가스유량, 액체 순환유량을 체크한 결과 혼합관의 길이가 길어지면 기-액 혼합 액체의 유로가 길어져 오존 가스가 반응액에 용해되기 쉬워 아세트아미노펜의 분해가 증가되지만 혼합관의 길이가 2.5 L/min이상에서는 반응기로 배출되는 오존 가스유량이 점차 감소하여 오존 가스유량을 2.5 L/min으로 유지하기 위하여 산소발생기로 유입되는 공기의 유량을 증가시켜야 하였다. 혼합관 길이가 3.0 m에서는 산소발생기의 유량이 6 ∼ 7 L/min이 필요하였으며, 3.0 m 이상에서는 공기 유량이 부족하여 실험이 불가능하였다. 따라서 관 길이 2.0 m 이상에서는 오존 발생장치의 성능에 영향을 주기 때문에 실험 시스템과 장치의 안정성을 위한 최적 혼합관 길이는 2.0 m인 것으로 판단되었다.
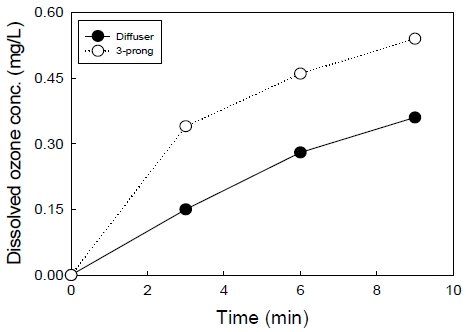
산기관과 3구 노즐을 이용한 조건에서 수중의 용존 오존농도를 측정하여 비교하였다. 산기관을 이용한 방법은 오존 발생장치 전력 120 W, 오존 가스유량 1.5 L/min, 오존 가스관 길이를 0.5 m로 유지한 조건에서 실험하였고, 혼합펌프와 노즐을 이용하는 오존 용존법은 3구 노즐, 액체 순환유량 1,914 mL/min, 오존 가스유량 1.5 L/min, 혼합관 길이 2 m인 조건에서 실험하여, 수중의 오존 농도를 Fig. 6에 나타내었다.
산기관을 이용하여 수중에 오존 가스를 배출시키는 경우 용존 오존농도는 반응 9분 후 0.36 mg/L로 나타났으나, 3구 노즐을 이용하는 경우 0.54 mg/L로 나타나, 용존 오존 농도가 1.5배 높아진 것으로 나타났다. 수중의 총잔류 산화제 농도를 나타내는 TRO (Total residual oxidants)를 측정한 결과, 용존 오존농도와 거의 유사한 농도를 나타내었다. 이는 오존 발생장치에서 발생하는 산화제 대부분이 오존이기 때문에 총잔류 산화제 농도가 오존 농도와 유사한 것으로 나타나 그래프로 나타내지는 않았다.
앞 절에서 구한 최적의 오존 용존 조건으로 오존을 공급하고 전기분해 공정을 추가 적용한 전기-페록손 공정에서 최적 운전을 위한 전기분해 공정의 최적의 전류량을 구하였다. Fig. 7에 변경된 오존의 공급방법을 적용한 오존 단일 공정과 전기-페록손 공정에서 전류 변화에 따른 생성 오존 농도(a)와 TRO 농도(b)를 나타내었다. 오존 단일공정의 오존 농도는 반응 12분에서 시간에 따라 선형적으로 증가하여 0.61 mg/L로 나타났다. 그러나 전기-페록손 공정의 경우 전류가 0.25 A에서 반응 12분 후 잔류 오존농도는 0.05 mg/L로 나타났고 1.0 A은 0.03 mg/L로 나타나 전류의 증가에 따라 용존 오존농도가 감소하는 경향을 나타내었으며 오존 단일공정에 비해 농도가 매우 낮게 나타났다.
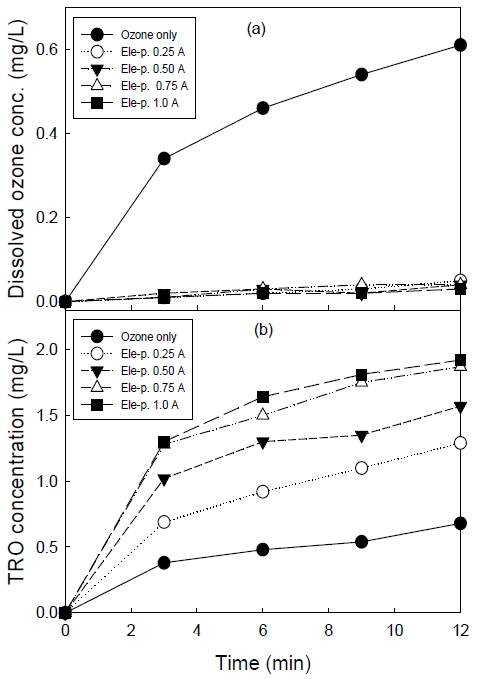
Comparison of dissolved ozone and TRO concentration with ozone process and electro-peroxone process.
Yoo and Kim(2011)은 3성분계 DSA 전극을 이용한 전기분해 공정에서 산화제 생성 실험에서 15분의 반응시간에서 과산화수소가 생성된다고 보고하였다. 이와 같이 전기분해 반응에서 생성된 과산화수소가 오존 발생장치에서 발생하는 오존과 반응하여 식 (1)과 같이 ·OH을 생성하는 전기-페록손 공정에서는 오존 발생장치에서 생성된 오존이 전기분해 공정에 의해 생성된 과산화수소와 반응하여 ·OH 생성에 거의 다 소모되기 때문에 수중의 잔류 오존농도가 Fig. 7(a)와 같이 낮은 것으로 생각되었다(Yu et al., 2013).
| (1) |
Fig. 7(b)에서는 수중에 존재하는 총 잔류 산화제 농도를 나타내는 TRO 농도를 나타내었다. TRO는 오존, 과산화수소는 물론 수중에 존재하는 모든 산화제 농도를 나타내기 때문에, TRO 농도가 높은 경우 수중에 존재하는 산화제 농도가 높다고 할 수 있다(Kim and Park, 2019).
오존 단일 공정의 경우 반응 12분 후 TRO 농도는 0.64 mg/L로 나타났고, 전기분해 공정을 적용한 전기-페록손 공정의 경우 0.25 A에서는 반응 12분 후 1.29 mg/L, 0.50 A에서는 1.57 mg/L, 0.75 A에서는 1.87 mg/L, 1.0 A에서는 1.92 mg/L로, 전류증가에 따라 TRO 농도가 선형적으로 증가하는 것으로 나타났고, 0.75 A와 1.0 A의 TRO농도 차이가 크지 않아 최적 전류는 0.75 A로 나타났다. 따라서 Fig. 7(a)에서 전기-페록손 공정의 낮은 오존 농도는 생성된 오존이 과산화수소와 반응하여 ·OH을 생성하기 때문에 오존 농도는 감소하지만 총 잔류 산화제 농도인 TRO 농도가 증가하였다고 판단되었다.
Fig. 8(a)에 오존 단일 공정과 전기-페록손 공정의 아세트아미노펜의 분해에 대해 나타내었다. 오존 공정의 경우 반응 12분 후 잔류 아세트아미노펜 농도는 3.14 mg/L(제거율, 68.6%)이었으며, 전기-페록손 공정에서는 전류가 0.25 A 인가될 때 12분에 100%가 제거되었고, 0.5 A 인가 시 반응 9분 후 잔류 아세트아미노펜 농도가 1.21 mg/L로 나타났고, 전류가 0.75 A과 1.0 A에서 반응 9분에 아세트아미노펜이 100% 제거되었다. 1.0 A의 초기 제거속도가 0.75 A보다 빠르지만 아세트아미노펜 제거율 100%에 도달되는 시간은 0.75 A와 1.0 A 모두 9분이므로 전기-페록손 공정에서 아세트아미노펜 분해에 대한 최적 전류는 0.75 A인 것으로 판단되었다. 이는 Fig. 7(b)의 TRO 생성 경향과 비슷한 것으로 나타났다,
아세트아미노펜의 분해가 완전 무기화를 의미하지는 않으므로 전기-페록손 공정에 의한 무기화를 고찰하기 위하여 Fig. 8(b)에 오존 공정과 전기-페록손 공정의 처리에 따른 TOC 농도 변화를 나타내었다. 오존 단독공정의 경우 TOC는 시간에 따라 거의 직선적으로 감소하는 경향을 나타내었고 180분 후 잔류 TOC 농도는 52.25 mg/L로 24.1%의 제거효율을 나타내었다. 전기-페록손 공정의 경우 0.25 A에서는 180분의 반응 후 잔류 TOC 농도는 34.5 mg/L로 49.8%의 제거율, 0.50 A는 18.7 mg/L(제거율 72.8%), 0.75 A는 7.8 mg/L(제거율 88.6%), 1.0 A는 6.01 mg/L(제거율 91.2%)로 나타났다. 아세트아미노펜 분해와 TOC 분해가 차이나는 것은 아세트아미노펜이 전기-페록손 공정을 통해 분해되면서 acetaminophen, hydroquinone, benzoquinone, hydroxyl acid, malonic acid 등의 중간산물을 거쳐 최종 무기화되기 때문에 이들 중간산물의 분해에 시간이 많이 소요되기 때문인 것으로 판단되었다(Kim, 2018).
3.2. 기존 전기-페록손 공정과의 성능 비교
산기관을 이용한 기존 전기-페록손 공정과 새로운 전기-페록손 공정과의 성능을 비교하기 위하여 같은 실험장치와 아세트아미노펜 농도를 이용한 Kim(2018)의 연구결과와 비교한 결과 아세트아미노펜 분해와 TOC 농도변화는 거의 유사한 결과를 나타내었다(data not shown). 두 공정의 정확한 성능 비교를 위하여 각 공정에서 사용한 전력소비량을 Table 1에 나타내었다. 기존 전기-페록손 공정은 메인 공정인 오존 공정의 오존 발생장치 표시 상 전력소비량이 140 Wh(전력량측정기로 측정한 실제 전력소비량, 130 Wh), 보조 공정인 전기분해 공정의 전력소비량은 1.44 Wh로 총 전력소비량은 131.44 Wh이었다. 본 연구는 오존 가스와 반응액을 순환펌프를 이용하여 미리 혼합한 뒤 반응기 내로 3구 노즐을 이용하여 배출시켜 오존의 용존율을 높였기 때문에 오존 공정의 전력소비량 120 Wh(실제 소비량, 92.6 Wh)로 줄였고 전기분해 공정의 전력소비는 3.23 Wh, 액체 순환펌프의 구동에 4.8 Wh를 이용하여 총 전력소비량은 100.36 Wh이었다. Fig. 9에 전력 소비량을 고려한 최적 조건에서 두 공정의 아세트아미노펜과 TOC 분해를 비교한 결과를 나타내었다.
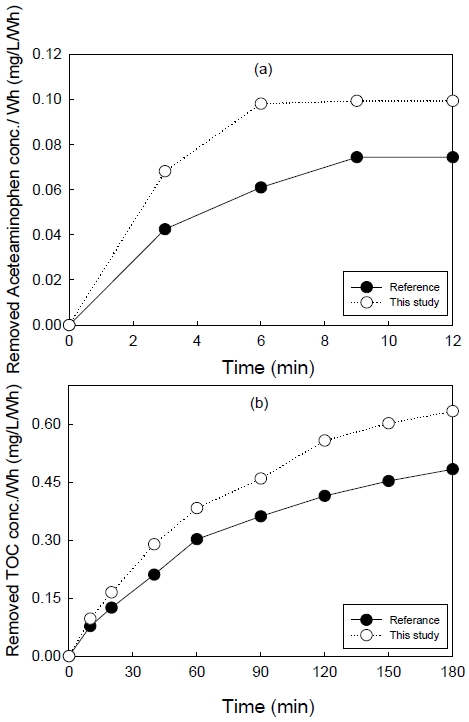
Comparison of Acetaminophen and TOC degradation per electric power power consumption with reference electro-peroxone process and this study.
Fig. 9(a)에 각각의 최적 조건에서 구한 아세트아미노펜 농도 변화를 나타내었다. Fig. 9(a)에 나타내었듯이 기존 전기-페록손 공정의 전력소비량 당 제거된 아세트아미노펜 농도는 9분에 0.074 mg/L/Wh로 나타났고, 본 연구에서는 0.099 mg/L/Wh로 나타나 본 연구의 전력소비량당 아세트아미노펜 제거는 1.33배 높은 것으로 나타났다.
Fig. 9(b)에서는 전력소비량 당 제거된 TOC 농도를 나타내었다. 기존 전기-페록손 공정은반응 180분에 TOC가 0.49 mg/L/Wh 제거되었고, 본 연구에서는 TOC 제거는 0.63 mg/L/Wh로 나타나 1.28배 높은 TOC 제거를 나타내었다. 따라서 전력소비량을 고려하지 않은 두 공정의 TOC 제거는 같이 나타났으나 오존 용존율을 높인 본 공정의 경우 액체 순환펌프의 전력소비가 추가되고 전기분해 공정의 전력소비가 증가하였으나 메인 공정인 오존 공정의 전력소비를 낮추어 전체 전력소비량이 76.55%로 낮아져 결과적으로 전력소비량당 TOC 제거가 높아졌다고 할 수 있다. 따라서 수중에서 오존 용존율을 높인 전기-페록손 공정이 낮은 전력소비량으로 아세트아미노펜을 무기화할 수 있는 것으로 판단되었다.
4. 결 론
오존 발생장치에서 발생하는 오존 가스를 산기관에서 오존 가스와 반응기 내의 반응액을 혼합시켜 노즐로 배출하여 오존의 용존율을 향상시킨 전기-페록손 공정의 성능을 평가하여 다음의 결과를 얻었다.
1. 오존 용존율 향상
1) 산기관을 이용하여 오존 가스를 수중에 직접 분사시키는 기존 방법보다 오존 가스-반응액을 혼합하여 3구 노즐로 분사시킨 경우의 아세트아미노펜 분해가 증가하는 것으로 나타났다. 최적 액체 순환유량은 1,914 mL/min이었고, 최적 오존 가스유량은 반응기 운전에 영향을 미치지 않는 오존 가스유량인 1.5 L/min이었다. 오존 가스와 반응액이 혼합되는 혼합관은 운전의 영향을 주지 않는 2.0 m가 최적인 것으로 판단되었다.
2) 3구 노즐을 이용하는 새로운 오존 용존법에 의한 오존 농도는 산기관을 이용하여 수중에 오존 가스를 배출시키는 기존 방법에 비해 용존 오존 농도가 1.5배 높아진 것으로 나타났다.
3) 오존 단일반응과 전기-페록손 공정의 비교
전기-페록손 공정에서 오존 농도가 오존 단일공정보다 낮은 것은 오존 공정에서 발생하는 오존과 전기분해 공정에서 발생하는 산화제 중 과산화수소가 반응하여 ·OH을 생성시켰기 때문인 것으로 감소한 것으로 판단되었다. 전기-페록손 공정에서 아세트아미노펜과 TOC 분해에 대한 최적 전류는 0.75 A로 나타났다. 아세트아미노펜 분해와 TOC 분해가 차이나는 것은 전기-페록손 공정에 의해 생성되는 중간산물의 분해에 시간이 많이 소요되기 때문인 것으로 판단되었다.
2. 기존 전기-페록손 공정과의 성능 비교
새로운 전기-페록손 공정의 전력소비량당 아세트아미노펜 제거는 기존 페록손 공정의 1.33배, TOC 제거는 1.28배 높은 것으로 나타났다. 오존 용존율을 높인 본 전기-페록손 공정은 기존 공정보다 낮은 전력소비량으로 아세트아미노펜을 무기화할 수 있는 것으로 판단되었다.
REFERENCES
-
Bader, H., Hoigné, J., 1981, Determination of ozone in water by the indigo method, Water Res., 15, 449-456.
[https://doi.org/10.1016/0043-1354(81)90054-3]

- Byeon, H. I., Yeo, G. H., Nguyen, A. H., Kim, Y. W., Kim, D. K., Lee, T. H., Jeong, S. H., Choi, Y. H., Oh, S. D., 2024, Potential of contaminant removal using a full-scale municipal water treatment system with adsorption as post-treatment, Land Hous. Rev., 15, 167-177.
-
Felisardo, R. J. A., Brillas, E., Boyer, T. H., Cavalcanti, E. B., Garcia-Segura, S., 2024, Electrochemical degradation of acetaminophen in urine matrices: Unraveling complexity and implications for realistic treatment strategies, Water Res., 261, 122034.
[https://doi.org/10.1016/j.watres.2024.122034]

-
Kim, D. S., Park, Y. S., 2018, Improvement of gas dissolution rate using air atomizing nozzle, J. Environ. Sci. Intl., 27, 63-74.
[https://doi.org/10.5322/JESI.2018.27.3.219]

- Kim, D. S., Park, Y. S., 2019, Derivation of optimal conditions for neutralization of residual oxides (TRO, Total residual oxidant), Proceedings of the Korean Environmental Sciences Society Conference, 100.
-
Kim, J. W., Ishibashi, H., Yamauchi, R., Ichikawa, N., Takao, Y., Hirano, M., Koga, M., Arizono, K., 2009, Acute toxicity of pharmaceutical and personal care products on freshwater crustacean (Thamnocephalus platyurus) and fish (Oryzias latipes), J. Toxicol. Sci., 34, 227-232.
[https://doi.org/10.2131/jts.34.227]

- Kim, U. Y., 2018, Decomposition of acetaminophen using electro-peroxone process, Master's thesis, Daegu Catholic University, Gyeongsangbuk-do, Korea.
-
Li, X., Wang, Y., Yuan, S., Li, Z., Wang, B., Huang, J., Deng, S., Yu, G., 2014, Degradation of the anti-inflammatory drug ibuprofen by electro-peroxone process, Water Res., 63, 81-93.
[https://doi.org/10.1016/j.watres.2014.06.009]

-
Park, S. J., Bin, J. I., Lee, E. S., Kim, I. S., 2010, Degradation and neutralization of total residual oxidant (TRO) in the treated ballast water by ozonation, J. Korean Soc. Mar. Eng., 34, 399-406.
[https://doi.org/10.5916/jkosme.2010.34.3.399]

-
Pashaei, R., Dzingelevičienė, R., Bradauskaitė, A., Lajevardipour, A., Mlynska-Szultka, M., Dzingelevičius, N., Raugelė, S., Razbadauskas, A., Abbasi, S., Rees, R. M., Buszewski, B., 2022, Pharmaceutical and microplastic pollution before and during the COVID-19 pandemic in surface water, wastewater, and groundwater, Water, 14, 1-18.
[https://doi.org/10.3390/w14193082]

-
Rashidi, R., Meraji, S. H., Mahmoudi, A., Sanati, A. M., Ramavandi, B., 2024, Enhanced catalytic degradation of acetaminophen using magnesium oxide-infused clay with ultrasonic activation of hydrogen peroxide, Arabian J. Chem., 17, 106047
[https://doi.org/10.1016/j.arabjc.2024.106047]

- Reyes, N. J., Geronimo, F. K., Guerra, H., Jeon, M. S., Choi, H. S., Lee, H. K., 2021, Pharmaceuticals and personal care products in wastewater: A Review of current research trends and treatment technologies, Korean Society of Water and Sewage · Korean Society of Water Environment, 2021 Joint Academic Presentation, 29-30.
-
Shokri, A., Nasernejad, B., 2024, Investigation of spent caustic effluent treatment by electro-peroxone process; cost evaluation and kinetic studies, J. Ind. Eng. Chem., 129, 170-179.
[https://doi.org/10.1016/j.jiec.2023.08.030]

- Water Encyclopedia, 2016, Ozone, http://www.water.or.kr, .
-
Yoo, Y. E., Kim, D. S., 2011, Comparison of dye removal performance and oxidants formation of insoluble electrode, J. Environ. Sci., 20, 1273-1284.
[https://doi.org/10.5322/JES.2011.20.10.1273]

-
Yu, H., Nie, Er., Xu, J., Yan, S. W., Copper, J. W., Song, W. H., 2013, Degradation of diclofenac by advanced oxidation and reduction processes : Kinetic studies degradation pathways and toxicity assessments, Water Res., 47, 1909-1918.
[https://doi.org/10.1016/j.watres.2013.01.016]

-
Zhang, J., Gong, D., Cheng, Z., 2024, Trace Ce(III) boosted acidic peroxone (O3/H2O2) process for efficient water treatment: Essential role of oxalic acid complexation, Sep. Purif. Technol., 351, 128088.
[https://doi.org/10.1016/j.seppur.2024.128088]

-
Zhang. G. Y., Sun, Y. B., Zhang, C. X., Yu, Z. Q., 2017, Decomposition of acetaminophen in water by a gas phase dielectric barrier discharge plasma combined with TiO2-rGO nanocomposite : Mechanism and degradation pathway, J. Hazard. Mater., 323, 719-729.
[https://doi.org/10.1016/j.jhazmat.2016.10.008]

-
Zhang, H., Cao, B., Liu W., Lin K. D., Feng, J., 2012, Oxidative removal of acetaminophen using zero valent aluminum-acid system : Efficacy, influencing factors, and reaction mechanism, J. Environ. Sci., 24, 314-319.
[https://doi.org/10.1016/S1001-0742(11)60769-9]

Division of Liberal Studies, Daegu Universityysparkk@daegu.ac.kr