여름철 제주도 하천과 하수처리장에서 검출된 과불화화합물 농도 및 분포 특성
Ⓒ The Korean Environmental Sciences Society. All rights reserved.
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
This study investigated the concentrations of fifteen per- and polyfluoroalkyl substances (PFAS) in rivers (perennial streams) and wastewater treatment plants (WWTPs) of Jeju Island during the summer of 2024, analyzing their environmental behavior and distribution. PFAS are highly stable in the environment and biota and are associated with potential toxic effects. In the perennial streams, perfluorohexanoic acid (PFHxA) and perfluorooctanoic acid (PFOA) were detected as the predominant compounds, with average concentrations of 0.77 ng/L and 0.33 ng/L, respectively. In WWTPs, PFOA, perfluoroheptanoic acid (PFHpA), and PFHxA were the dominant substances, with average concentrations of 1.71 ng/L, 0.58 ng/L, and 0.81 ng/L, respectively. The detected PFAS concentrations were below domestic and international drinking water standards, indicating relatively safe levels. However, the necessity of long-term environmental monitoring is emphasized to ensure sustained environmental safety. This study provides baseline data for understanding PFAS behavior and underscores the importance of continuous monitoring to mitigate potential risks.
Keywords:
PFAS, WWTP, River, Monitoring, Jeju1. 서 론
과불화화합물(Per- and polyfluoroalkyl substances: PFAS)은 탄소-불소(C-F)의 강력한 결합으로 인해 환경 중에서 쉽게 분해되지 않는 인공 유기불소화합물 그룹이다(Buck et al., 2011). ‘영원한 화학물질’로도 불리는 PFAS는 탁월한 지속성, 생물 농축성, 그리고 수계 환경에서의 광범위한 이동성으로 인해 전 지구적 환경 문제로 대두되고 있다(Herzke et al., 2012). 이 물질은 수성막포소화약제, 반도체 및 전자 산업 공정, 그리고 식품 포장재, 방수 의류 등 다양한 소비재에 이르기까지 광범위하게 사용되어 왔으며, 이러한 배출원으로부터 환경으로 유출되어 하천, 호수, 지하수, 토양뿐만 아니라 야생동물과 인체에서도 검출되고 있다(Giesy and Kannan, 2002; Prevedouros et al., 2006).
다양한 환경 매체 중 수계 환경은 오염물질의 주요 이동 경로이자 인간 노출의 핵심 매개체로 작용한다. 특히 먹는 물을 통한 인체 노출은 PFAS의 잠재적 독성과 관련하여 공중 보건의 주요 관심사로 부상하였으며, 이에 따라 미국 환경보호청(US EPA)과 유럽연합(EU) 등 세계 각국은 먹는 물 중 PFAS에 대한 규제 및 권고 기준을 강화하는 추세이다(Brennan et al., 2021). 국내에서도 환경부를 중심으로 과불화옥탄산(Perfluorooctanoic acid: PFOA), 과불화옥탄술폰산(Perfluorooctane sulfonate: PFOS)과 과불화헥산술폰산(Perfluorohexane sulfonic acid: PFHxS)을 먹는 물 수질 감시항목으로 지정하여 관리하는 등 그 중요성을 인식하고 있다(MOE, 2025).
그러나 국제적으로 PFAS 규제가 강화되는 추세에도 불구하고, 국내의 PFAS 규제 수준은 상대적으로 완화된 상태에 머물러 있다(Kim et al., 2025). 환경부는 2018년 먹는물 관리 기준으로 PFOA와 PFOS 합계 70 ng/L, PFHxS 480 ng/L 이하로 농도를 설정하였으나, 이는 국제 기준과 비교할 때 상대적으로 높은 수준으로 평가된다(Kang et al., 2025). EU는 2013년 제정된 Directive 2013/39/EU를 통해 PFOS에 대한 내륙 지표수 기준을 0.65 ng/L로 설정하였으며, 2020년 Directive 2020/2184에서는 음용수 내 PFAS 총량 규제를 도입하여, 총 농도 500 ng/L, 특정 구조 물질의 합계 100 ng/L 기준을 마련하였다(EP&CEU, 2020). US EPA는 2024년 발표한 최종 음용수 기준(National Primary Drinking Water Regulation: NPDWR)을 통해, PFOS와 PFOA에 대해 각각 4 ng/L, PFHxS와 Perfluorononanoic acid (PFNA)에 대해 각각 10 ng/L의 매우 엄격한 기준을 설정하였다(US EPA, 2024). 일본 보건복지부 역시 PFOS와 PFOA 합계 기준을 50 ng/L로 규정하고 있다(MHLW, 2020). 이러한 국제적 기준과의 차이는 국내 PFAS 규제가 개선될 필요가 있음을 시사한다(Takagi et al., 2008).
또한, 제주도는 대부분 투수성이 높은 현무암질 암반으로 형성되어 있으며, 이러한 지질학적 특성으로 인해 지표에서 유입된 오염물질은 토양층의 자연 정화 과정을 충분히 거치지 않고 신속하게 지하수계로 이동하는 구조적 취약성을 보인다(Jung et al., 2014). 게다가 제주도민이 사용하는 생활용수 및 음용수의 90% 이상을 지하수에 의존하고 있어, 지하수의 오염은 도민의 건강과 안전에 위협이 될 수 있다. 제주국제공항에서의 소방훈련 활동, 인구 증가 및 관광객 급증에 따른 하수처리시설 부하 증가, 다수의 폐기물 매립지 등은 제주도 내 PFAS의 잠재적 배출원으로 고려될 수 있다. 그럼에도 불구하고, 제주도의 이러한 특수성을 고려하여 섬 전역의 다양한 수계(하천, 용천수, 연안, 지하수)를 아우르는 PFAS 오염 실태와 분포 특성에 대한 체계적이고 종합적인 연구는 아직 미흡한 실정이다.
본 연구는 제주도 내 주요 하수처리장의 유입수와 방류수, 그리고 하천수에서 검출되는 PFAS의 농도 수준과 공간적 분포 특성을 규명하는 것을 목적으로 수행되었다. 이를 위해 하수처리 공정 전후와 하천에서 시료를 채취하여 주요 PFAS 물질의 농도 변화와 거동을 분석하였다. 세부 목표는 (1) 제주도 내 주요 수계에서 PFOA, PFOS를 포함한 주요 PFAS의 농도 수준과 검출 특성을 파악하고, (2) 수계별·지역별 오염도 차이를 비교하여 공간적 분포 특성을 규명하며, (3) 이를 바탕으로 PFAS의 잠재적 오염원을 추론하는 것이다. 연구 결과는 하수처리 과정에서의 PFAS 제거 효율을 평가하고, 방류수가 하천 생태계에 미치는 영향을 정량적으로 파악하는 데 기여할 수 있다. 궁극적으로 본 연구는 제주특별자치도의 청정 수자원 보전과 PFAS 관리 방안 수립을 위한 과학적 근거를 제공할 것이다.
2. 재료 및 방법
2.1. 시료채취
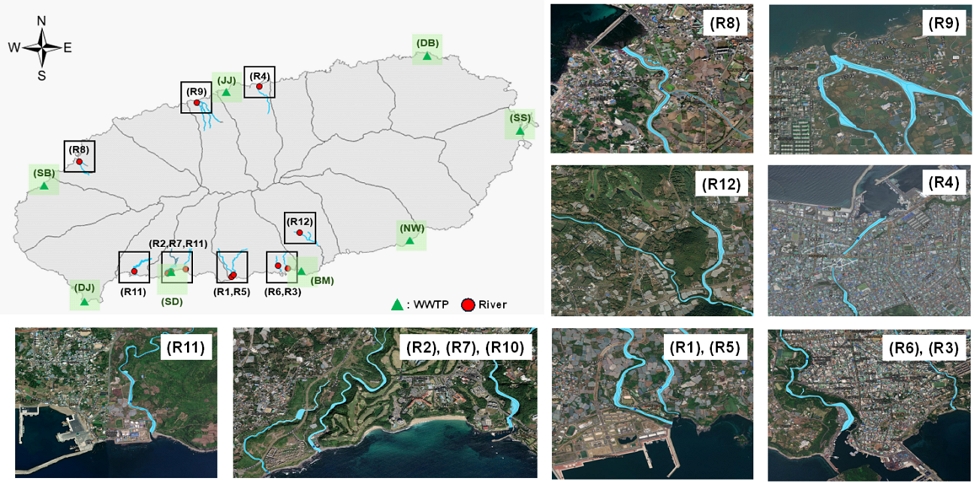
본 연구에서 상시천 시료는 제주보건환경연구원에서 분기별 하천수 수질조사를 진행하는 상시천 12지점을 대상으로 시료를 각 1회 채취하였으며, 하수처리장의 경우 제주도 공공하수처리장 8곳을 대상으로 유입수와 방류수 시료를 채취하였다(Fig. 1). 시료채취는 월별 농도 변화를 확인하기 위해 2024년 6월과 8월에 Polypropylene 재질의 2 L 채수병을 사용하고, 시료 채취에 필요한 모든 도구는 테플론과 초자기구 사용을 배제하였다. 채수 시에는 대상 시료를 이용하여 2회 이상 반복 세척한 뒤 사용하였고, 채취된 시료는 전처리 전까지 냉장보관(4°C) 하였다.
2.2. 분석대상 물질과 시약
본 연구에서는 제주도의 상시천 및 하수처리장 시료를 대상으로 총 15종의 PFAS를 분석하였다. 분석대상 물질은 스톡홀름 협약과 주요 국가 규제에서 잔류성유기오염물질(Persistent organic pollutants: POPs)로 지정된 화합물인 PFOA, PFOS, PFHxS를 비롯하여 기존의 규제된 PFAS를 대체하기 위해 사용이 증가하고 있는 Chlorinated polyfluorinated ether sulfonic acid (F-53B)와 같은 대체물질도 포함하여 Perfluoroalkyl carboxylic acids (PFCAs) 9종[Perfluorohexanoic acid (PFHxA), Perfluoroheptanoic acid (PFHpA), PFOA, PFNA, Perfluorodecanoic acid (PFDA), Perfluoronudecanoic acid (PFUnDA), Perfluoroundecanoic acid (PFDoDA), Perfluorotridecanoic acid (PFTrDA), Perfluorotetradecanoic acid (PFTeDA)], Perfluoroalkane sulfonic acids (PFSAs) 2종[PFHxS, PFOS], Intermediates 2종[N-methyl perfluorooctane sulfonamido acetic acid (N-MeFOSAA), N-ethyl perfluorooctane sulfonamido acetic acid (N-EtFOSA)], Alternative 2종[9-Chlorohexadecafluoro-3-oxanonane-1-sulfonic acid (9Cl-PF3ONS), 11-Chloroeicosafluoro-3-oxaundecane-1-sulfonic acid (11Cl-PF3OUdS)]으로 총 15종을 분석대상물질로 선정하였다. 표준물질 및 내부표준물질은 Wellington Laboratories사(Canada)에서 혼합물질로 만들어진 고순도 시약을 구입하였으며, 메탄올과 물은 J.T. Baker 사(NJ, USA)의 HPLC 등급 시약을 사용하였다. 아세트산암모늄(CH3COONH4) 용액은 Junsei 사(Japan) 특급 시약을 사용하였으며, 수산화암모늄(NH4OH, 28% NH3 in H2O) 용액은 Sigma-Aldrich 사(USA)의 고순도 시약을 사용하였다.
2.3. 전처리와 기기분석
시료의 전처리 방법은 잔류성유기오염물질공정시험기준(ES 10363.1a)을 바탕으로 시험하였으며, 전처리 과정 중 과불화화합물이 유리 표면에 흡착될 수 있는 특성을 고려하여 초자 기구의 사용을 배제하였다. 채수된 각 시료는 500 mL를 PES필터(0.22 μm PES Membrane filter)를 이용하여 여과를 거친 후 사용하였다. 여과 후 회수율을 확인하기 위해 정제용 내부표준물질 표준용액 5 ng (0.1 ng/μL 조제 용액 50 μL)을 주입하였다. 추출과 농축을 위해 Oasis WAX (6 cc, 150 mg, Waters, USA)카트리지를 0.1% 수산화암모늄 포함 메탄올 용액, 메탄올, 물을 각각 4 mL로 활성화시킨 후 시료를 10~15 mL/min의 유속으로 통과시켰다. 시료를 모두 통과시킨 카트리지는 25 mM 아세트산암모늄 용액 4 mL로 세척 후 진공을 걸어 30분간 건조하고 메탄올 4 mL씩 2회 용리(Elution)하였다. 용리된 시료는 질소농축기(MG2200, Eyela, Japan)를 이용하여 0.5 mL이하로 농축하고, 0.2 μm 실린지 필터 여과하였다. 이후, 첨가용 내부표준물질을 5 ng 주입하고 메탄올을 사용하여 최종 부피가 1 mL가 되도록 하였다(Fig. 2).
분석에 사용한 장비는 Waters (USA)사의 액체크로마토그래피-텐덤질량분석기(Liquid Chromatograph-Tandem Mass Spectrometer: LC-MS/MS)를 사용했으며, ACQUITY UPLC Binary Solvent Manager와 연결된 Xevo TQ-S triple quadrupole mass spectrometer를 검출기로 사용하였다. 분석컬럼은 2.1 × 50 mm (1.7 µL) ACQUITY UPLC BEH C18을 사용하였고, 이동상은 2 mM 암모늄 아세테이트(용매 A)와 메탄올(용매 B)을 선택하였다. Gradient조건은 초기 95% A와 5% B로 시작하여 시간에 따라 비율을 변화하였다. 전자분무이온화(Electrospray ionization, ESI)방법으로 시료를 이온화 하였고, 각 대상 물질에 대해 전구이온(Precursor ion, PI)과 정량/정성이온(Quantification/Qualification ion, QI1/QI2)을 각각 선정하여 다중 반응 모니터링(Multiple reaction monitoring, MRM)으로 분석하였다.
본 연구에서 사용된 실험방법의 신뢰성을 평가하기 위해 품질 관리 절차를 「잔류성유기오염물질 공정시험기준 ES 10001.a 정도보증/정도관리」에 따라 수행하였다. 모든 분석 대상 화합물에 대해 방법 검출 한계(Method detection limit: MDL)와 정량 한계(Limit of quantitation: LOQ)를 결정하고, 실험의 반복성을 검증하기 위해 공시료를 7회 반복 분석하였다. MDL은 표준편차에 99% 신뢰도를 가지는 Student's t값(3.14)을 곱하여 산출하였다. MDL 값은 0.075 ng/L (PFOA)에서 0.317 ng/L (11Cl-PF3OUdS) 범위로 나타났으며, 상대 표준편차는 10% 이하로 정밀도에 적합한 수준을 보였다. 또한, 전체 평균 회수율은 89.4%로 70∼110% 범위 내에 포함되어 전반적으로 양호하였다. 분석 대상 화합물의 정량을 위해 0.5~50 ng/mL 범위의 검정곡선을 작성하였고, 검량선의 상관계수(R2)는 모든 화합물에서 0.99 이상의 높은 직선성을 나타내었다.
3. 결과 및 고찰
3.1. PFAS의 농도 수준
본 연구에서는 제주도 상시 하천 및 하수처리장에서 PFAS 15종의 농도를 분석하였으며, 그 결과 9종(9Cl-PF3ONS, PFDA, N-MeFOSAA, N-EtFOSAA, PFUnDA, 11Cl-PF3OUdS, PFDoDA, PFTrDA, PFTeDA)은 모든 지점에서 불검출(Not detected: ND)로 확인되었다. 반면, PFHxA, PFHpA, PFHxS, PFOA, PFNA, PFOS는 일부 시료에서 검출되었으며, 이들 중 PFHxA와 PFOA가 상대적으로 높은 농도를 보였다. PFAS 15종 중 검출된 PFHxA는 ND~7.82 ng/L, PFHpA는 ND~4.83 ng/L, PFHxS는 ND~1.01 ng/L, PFOA는 ND~10.04 ng/L, PFNA는 ND~2.08 ng/L, PFOS는 ND~1.40 ng/L로 나타났다. 검출된 6종의 PFAS 중 PFHxA와 PFOA가 연구 대상 지역에서 주된 PFAS 오염 물질로 작용할 가능성이 높음을 시사한다. 특히, PFHxA는 6월에 전체 검출량의 79 ± 17%, 8월에 51 ± 34%를 차지하였으며, PFOA는 6월에 18 ± 17%, 8월에 35 ± 32%를 차지하여 상대적으로 높은 검출 비율을 보였다(Fig. 3).
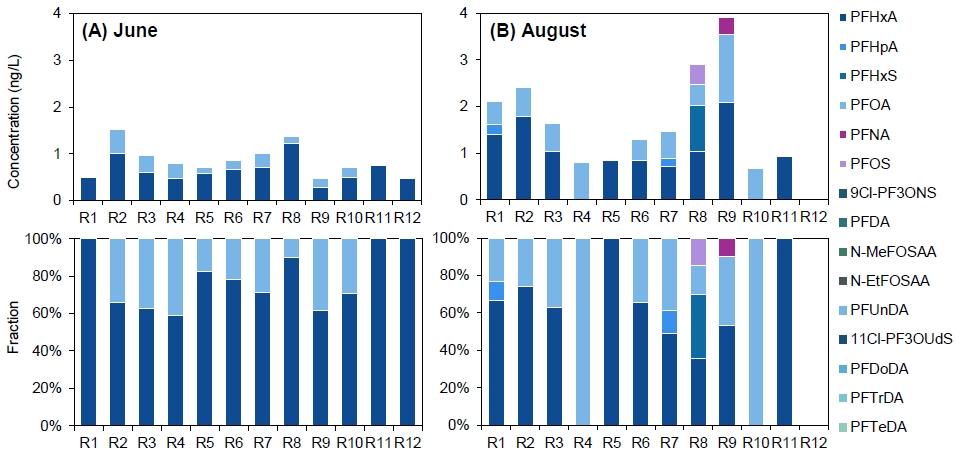
Concentrations and fraction of PFAS at sampling stations (12 perennial streams) in (A) June and (B) August.
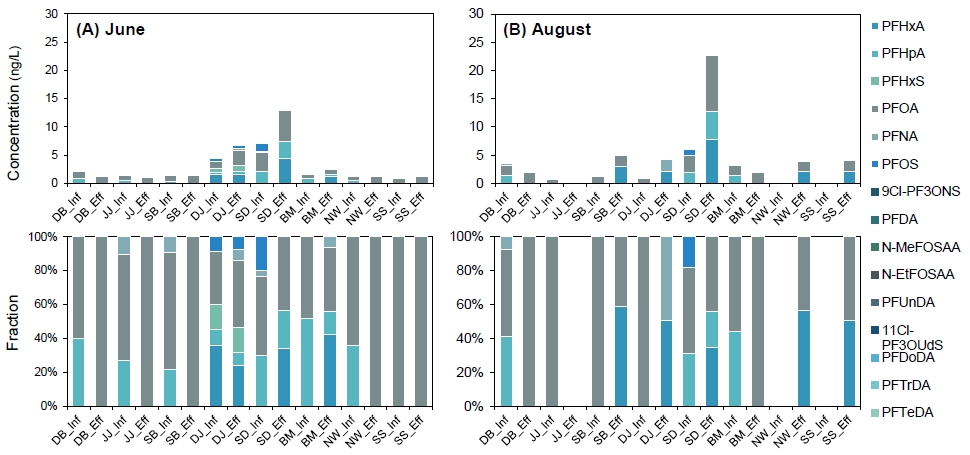
하수처리장 유입수에서의 PFAS 농도는 시기별로 검출 항목과 농도 수준에 차이를 보였다. 6월의 경우, PFAS 6종(PFHxA, PFHpA, PFHxS, PFOA, PFNA, PFOS)이 검출되었으며, 농도 범위는 PFHxA ND∼1.56 ng/L, PFHpA ND∼2.09 ng/L, PFHxS ND∼0.62 ng/L, PFOA 0.72∼3.30 ng/L, PFNA ND∼0.25 ng/L, PFOS ND∼1.40 ng/L로 나타났다(Fig. 4). 8월에는 PFHxA와 PFHxS가 검출되지 않았고, PFAS 4종(PFHpA, PFOA, PFNA, PFOS)은 6월과 유사한 농도 수준으로 확인되었다. 방류수에서도 유입수와 유사한 물질들이 검출되었으나, 검출 항목과 농도 수준은 시기와 물질별로 차이를 보였다. 6월 방류수에서는 PFAS 6종이 검출되었으며, 농도 범위는 PFHxA ND∼4.40 ng/L, PFHpA ND∼2.92 ng/L, PFHxS ND∼1.01 ng/L, PFOA 1.02∼5.64 ng/L, PFNA ND∼0.43 ng/L, PFOS ND∼0.50 ng/L로 나타났다. 8월 방류수에서는 PFHxS와 PFOS가 검출되지 않았고, 유입수에서 검출되지 않았던 PFHxA가 5개 지점(SB, DJ, SD, NW, SS) 방류수에서 검출되었다(PFHxA ND∼7.82 ng/L, PFHpA ND∼4.83 ng/L, PFOA ND∼10.04 ng/L, PFNA ND∼2.08 ng/L). 전반적으로 방류수의 PFAS 농도는 유입수보다 높거나, 유입수에서는 검출되지 않았던 물질이 새롭게 검출되는 경향을 보였다. 이는 해당 시기 유입수에 전구체 물질이 상대적으로 많이 존재하였고, 하수처리 공정 내 산화 및 생물학적 반응을 통해 전환되었을 가능성을 시사한다(Lenka et al., 2021). 선행연구에 따르면, 6:2 Fluorotelomer sulfonic acid (FTS)와 같은 텔로머 기반 전구체는 호기성 조건에서 PFHxA 등 단쇄성 PFCAs로 생물학적 전환될 수 있음이 보고되었다(Zhang et al., 2016; Hamid et al., 2020). 또한, 계절에 따라 강수량과 지표면 유출량이 달라짐에 따라 PFAS의 유입 경로와 유입량이 변화하며, 이는 시기별 농도 차이로 이어질 수 있다.
3.2. 선행연구와의 비교
국내 내륙 지역 하천에서의 선행연구 결과에 따르면, 금강, 낙동강, 남강, 남한강, 북한강 등 주요 하천에서 PFAS 농도는 항목에 따라 1 ng/L 이하에서 수십 ng/L에 이르는 다양한 범위를 나타내었으며, 일부 지점에서는 30∼40 ng/L 수준의 고농도 사례도 보고되었다. 금강에서는 PFOA가 최대 39.7 ng/L, PFOS가 최대 48.4 ng/L까지 검출되었고, 남한강에서는 PFHxA가 최대 26.5 ng/L로 확인되었다(Table 1).
반면, 본 연구에서 조사한 제주 지역 하천의 PFAS 농도는 평균적으로 1 ng/L 이하이거나 대부분 ND로 나타났다. 6월, 8월 채취한 시료 분석 결과, PFHxA의 평균 농도는 0.89 ng/L, PFOA는 0.51 ng/L, PFOS는 0.04 ng/L 수준으로 나타났으며, 이는 국내 선행연구에서 보고된 다른 지역 하천 내 평균값보다 낮은 수준이다. 특히, 일부 항목(PFHpA, PFHxS, PFNA, PFOS)은 6월 시료에서 ND로 나타나 다른 지역 하천과 뚜렷한 차이를 보였다. 이러한 결과는 제주 지역 하천의 수문지질학적 특성과 오염원 분포가 내륙 지역과 상이함을 보여준다.
국내 하수처리장 내 PFAS 농도는 지역별 차이를 보였고, 다수 항목에서 수 ng/L에서 수십 ng/L까지 농도 수준이 보고되었다(Table 2). 서울의 하수처리장 방류수에서 PFOA는 최대 580 ng/L(평균 215 ng/L), PFOS는 최대 264 ng/L(평균 145.17 ng/L)로 나타났으며, 전주 지역 유입수에서도 PFHxS 및 PFOS가 각각 평균 22.12 ng/L, 21.76 ng/L로 검출되었다. 제주도에서도 2015년 연구에서는 PFHxA, PFHxS, PFOA가 3∼5 ng/L 이상 검출된 사례가 있었다. 그러나 본 연구 결과에서는 제주 지역 하수처리장의 PFAS 농도가 전반적으로 낮은 수준으로 나타났으며, 대부분의 항목은 평균 0.1∼2 ng/L 범위였다. 이는 계절적 배출원 변화, 처리 효율 저하, PFAS의 재형성의 영향을 시사하며, PFAS의 계절적 거동 특성을 고려한 장기적이고 지속적인 모니터링이 필수적임을 보여준다.
4. 결 론
본 연구는 제주특별자치도 내 주요 하천수 중 12지점의 상시천과 8개 공공하수처리장을 대상으로 여름철 PFAS의 농도를 확인하였다. 하천수 분석 결과, PFHxA와 PFOA가 전 지점에서 가장 빈번하게 검출되었으며, 두 물질이 제주 지역 상시천 내 PFAS 오염의 주요 구성 성분임을 확인하였다. 국내 주요 하천을 대상으로 한 선행연구에서도 PFHxA, PFOA, PFOS는 88∼100%의 높은 검출 빈도를 보였으며, PFAS 사용이 감소 추세임에도 여전히 환경 내 주요 오염원으로 작용하고 있음을 시사한다.
하수처리장 유입수와 방류수에서도 PFHxA와 PFOA가 대부분의 지점에서 공통적으로 검출되어 주요 오염물질로 확인되었다. 방류수의 경우, 유입수보다 PFAS 농도가 높거나, 유입수에서는 검출되지 않던 항목이 새롭게 검출되는 경우가 다수 나타났다. 이는 하수처리 공정 중 PFAS가 완전히 제거되지 않거나, 전구체로부터 전환되어 재출현될 가능성을 시사한다. 하수처리 공정의 유형 및 운전 조건은 PFAS의 제거 효율에 영향을 미치며, 공정 간 차이가 농도 수준에 반영될 수 있다. 따라서, PFAS 농도의 물질별·시기별 차이는 이와 같은 다양한 요인의 복합적 영향에 기인한 것으로 해석된다.
본 연구는 국내에서 PFOS 및 PFOA의 먹는물 수질감시기준이 수립된 2018년 이후, 제주 지역 내 주요 하천과 공공하수처리장을 대상으로 PFAS 농도와 환경적 특성을 조사하였다. 특히, 하수처리 공정에서의 방류수에 의한 재오염 가능성을 모니터링 분석자료를 통해 확인함으로써, 제주 지역 내 PFAS의 환경적 특성을 파악하였다. 향후, PFAS 오염특성을 더 정확히 파악하고 실효성 있는 정책제언을 위해서는 PFAS 전구체에 대한 장기적인 모니터링과 처리 공정 내 제거 효율 평가 등 보다 심층적인 후속 연구를 수행해야 한다.
Acknowledgments
본 연구는 2025년도 교육부 및 제주도의 재원으로 제주RISE센터의 지원을 받아 수행된 지역혁신중심 대학지원체계(RISE)의 결과입니다(2025-RISE-17-001).
REFERENCES
-
Brennan, N. M., Evans, A. T., Fritz, M. K., Peak, S. A., von Holst, H. E., 2021, Trends in the regulation of per-and polyfluoroalkyl substances (PFAS): A Scoping review, Int. J. Environ. Res. Public Health, 18, 10900.
[https://doi.org/10.3390/ijerph182010900]

-
Buck, R. C., Franklin, J., Berger, U., Conder, J. M., Cousins, I. T., De Voogt, P., Jensen, A. A., Kannan, K., Mabury, S. A., Van Leeuwen, S. P., 2011, Perfluoroalkyl and polyfluoroalkyl substances in the environment: terminology, classification, and origins, Integr. Environ. Assess. Manag., 7, 513–541.
[https://doi.org/10.1002/ieam.258]

- EP & CEU (European Parliament and Council of the European Union), 2020, Directive (EU) 2020/2184 of the European Parliament and of the Council, Directive (No. 2184), Brussels, Belgium.
-
Giesy, J. P., Kannan, K., 2002, Peer reviewed: Perfluorochemical surfactants in the environment, Environ. Sci. Technol., 36, 146A–152A.
[https://doi.org/10.1021/es022253t]

-
Guo, R., Sim, W. J., Lee, E. S., Lee, J. H., Oh, J. E., 2010, Evaluation of the fate of perfluoroalkyl compounds in wastewater treatment plants, Water Res., 44, 3476–3486.
[https://doi.org/10.1016/j.watres.2010.03.028]

-
Hamid, H., Li, L. Y., Grace, J. R., 2020, Formation of perfluorocarboxylic acids from 6: 2 fluorotelomer sulfonate (6: 2 FTS) in landfill leachate: Role of microbial communities, Environ. Pollut., 259, 113835.
[https://doi.org/10.1016/j.envpol.2019.113835]

-
Herzke, D., Olsson, E., Posner, S., 2012, Perfluoroalkyl and polyfluoroalkyl substances (PFASs) in consumer products in Norway–a pilot study, Chemosphere, 88, 980–987.
[https://doi.org/10.1016/j.chemosphere.2012.03.035]

-
Jung, H. W., Yun, S. T., Kim, K. H., Oh, S. S., Kang, K. G., 2014, Role of an impermeable layer in controlling groundwater chemistry in a basaltic aquifer beneath an agricultural field, Jeju Island, South Korea, Appl. Geochem., 45, 82–93.
[https://doi.org/10.1016/j.apgeochem.2014.03.008]

- Kam, S. K., Baek, B. C., Kim, K. S., 2016, A Study on the presence of perfluorinated compounds (PFCs) in the public sewage treatment plants - case of Jeju Province sewage treatment plants, J. Korean Soc. Urban Environ., 16, 35–45.
-
Kang, J. K., Kim, M. G., Oh, J. E., 2025, Occurrence and removal of 42 legacy and emerging per-and polyfluoroalkyl substances (PFAS) in drinking water treatment plants in South Korea, Water Res. X, 29, 100329.
[https://doi.org/10.1016/j.wroa.2025.100329]

-
Kim, Y., Cho, A. H., Seo, Y. E., Kho, Y., Choi, K., 2025, Occurrence of per- and polyfluoroalkyl substances (PFAS) in potable groundwater near military bases in South Korea, Environ. Sci. Technol. Lett., 12, 440–446.
[https://doi.org/10.1021/acs.estlett.5c00105]

-
Lam, N. H., Cho, C. R., Lee, J. S., Soh, H. Y., Lee, B. C., Lee, J. A., Tatarozako, N., Sasaki, K., Saito, N., Iwabuchi, K., 2014, Perfluorinated alkyl substances in water, sediment, plankton and fish from Korean rivers and lakes: A Nationwide survey, Sci. Total Environ., 491, 154–162.
[https://doi.org/10.1016/j.scitotenv.2014.01.045]

-
Lee, I. J., Yoon, W. H., Jeong, G. J., Cho, S. J., 2024, Distribution and risk assessment of perfluoroalkyl and polyfluoroalkyl substances (PFAS) in the South Han River, J. Environ. Anal. Health Toxicol., 27, 29–38.
[https://doi.org/10.36278/jeaht.27.1.29]

-
Lenka, S. P., Kah, M., Padhye, L. P., 2021, A Review of the occurrence, transformation, and removal of poly-and perfluoroalkyl substances (PFAS) in wastewater treatment plants, Water Res., 199, 117187.
[https://doi.org/10.1016/j.watres.2021.117187]

- MHLW (Ministry of Health, Labour and Welfare), 2020, Implementation guidelines regarding the partial revision of the ordinance on drinking water quality standards, Official Notice (No. 0330-2), Tokyo, Japan.
- MOE (Ministry of Environment), 2025, Notice on the operation of drinking water quality monitoring items, Official Notice (No. 2025-165), Sejong, South Korea.
-
Naile, J. E., Khim, J. S., Wang, T., Chen, C., Luo, W., Kwon, B. O., Park, J., Koh, C. H., Jones, P. D., Lu, Y., 2010, Perfluorinated compounds in water, sediment, soil and biota from estuarine and coastal areas of Korea, Environ. Pollut., 158, 1237–1244.
[https://doi.org/10.1016/j.envpol.2010.01.023]

-
Park, J. E., Kim, S. K., Oh, J. K., Ahn, S. Y., Lee, M. N., Cho, C. R., Kim, K. S., 2012, Study on concentrations and mass flows of perfluorinated compounds (PFCs) in a wastewater treatment plant, J. Korean Soc. Environ. Eng., 34, 326–334.
[https://doi.org/10.4491/KSEE.2012.34.5.326]

-
Prevedouros, K., Cousins, I. T., Buck, R. C., Korzeniowski, S. H., 2006, Sources, fate and transport of perfluorocarboxylates, Environ. Sci. Technol., 40, 32–44.
[https://doi.org/10.1021/es0512475]

-
Shin, M., Im, J., Kho, Y., Choi, K., Zoh, K., 2009, Quantitative determination of PFOA and PFOS in the effluent of sewage treatment plants and in Han River, J. Environ. Health Sci., 35, 334–342.
[https://doi.org/10.5668/JEHS.2009.35.4.334]

-
Takagi, S., Adachi, F., Miyano, K., Koizumi, Y., Tanaka, H., Mimura, M., Watanabe, I., Tanabe, S., Kannan, K., 2008, Perfluorooctanesulfonate and perfluorooctanoate in raw and treated tap water from Osaka, Japan, Chemosphere, 72, 1409–1412.
[https://doi.org/10.1016/j.chemosphere.2008.05.034]

- US EPA (U.S. Environmental Protection Agency), 2024, PFAS national primary drinking water regulation, Regulation Report (No. 2024-07773), Washington, D.C., USA.
-
Yeo, M. K., Hwang, E. H., Jeong, G. H., 2012, Distribution characteristics of perfluorinated compounds in major river water and sediment, Anal. Sci. Technol., 25, 313–323.
[https://doi.org/10.5806/AST.2012.25.5.313]

-
Zhang, S., Lu, X., Wang, N., Buck, R. C., 2016, Biotransformation potential of 6: 2 fluorotelomer sulfonate (6: 2 FTSA) in aerobic and anaerobic sediment, Chemosphere, 154, 224–230.
[https://doi.org/10.1016/j.chemosphere.2016.03.062]

Department of Environmental Engineering, Jeju National Universitymkpark@jejunu.ac.kr
Department of Environmental Engineering, Jeju National Universityans2390@naver.com